
分析 (1)由N2H4的量,并据方程式2NH3~N2H4关系,求NH3的体积;
(2)①由H2O2+NaClO=NaCl+O2+H2O方程式,并根据单质,氧化物不拆,强酸,强碱,大多数盐拆来书写离子方程式;
②据H2O2受热易分解来分析;
③根据Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O求得与K2Cr2O7反应的Fe2+,n(Fe2+)1=2×10-4 mol×6=1.2×10-3 mol,则与ClO3-反应的Fe2+,n(Fe2+)2=0.1000 mol•L-1×30.00×10-3 L-1.2×10-3 mol=1.8×10-3 mol,并根据ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O计算NaClO3的量,并求得其含量.
解答 解:(1)m(N2H4)=m(N2H4)w=1000×25.6%=256g
n(N2H4)=$\frac{m({N}_{2}{H}_{4})}{M}$=$\frac{256}{32}$=8mol
NaClO+2NH3═N2H4+NaCl+H2O
2×22.4 1
V 8
$\frac{2×22.4}{V}$=$\frac{1}{8}$;V=358.4L
故答案为:358.4;
(2)①用H2O2与次氯酸钠反应为H2O2+NaClO=NaCl+O2↑+H2O,离子方程式为H2O2+ClO-=Cl-+O2↑+H2O,
故答案为:H2O2+ClO-=Cl-+O2↑+H2O;
②因为H2O2受热易分解故加热煮沸的目的是除去过量的H2O2,
故答案为:除去过量的H2O2;
③n(K2Cr2O7)=0.01000 mol•L-1×20.00×10-3 L=2×10-4 mol
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
1 6
2×10-4 1.2×10-3
∴与K2Cr2O7反应的Fe2+为n(Fe2+)1=2×10-4 mol×6=1.2×10-3 mol
∴与ClO3-反应的Fe2+为n(Fe2+)2=0.1000 mol•L-1×30.00×10-3 L-1.2×10-3 mol=1.8×10-3 mol
ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O
1 6
3×10-4 1.8×10-3
∴在10 mLNaClO3溶液试样中:n(NaClO3)=3×10-4 mol
∴样品中NaClO3的含量=$\frac{3×1{0}^{-4}mol×165.5g/mol}{10×1{0}^{-3}L}$=3.195 g•L-1
答:样品中NaClO3的含量为3.195 g•L-1.
点评 本题考查物质制备实验,涉及离子方程式书写,氧化还原反应,以及信息获取与运用等,侧重学生综合应用能力,题目难度中等,明确实验目的,实验原理为解答关键.


科目:高中化学 来源: 题型:解答题
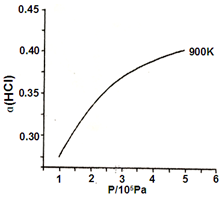 氯及其化合物在生活和生产中应用广泛.
氯及其化合物在生活和生产中应用广泛.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
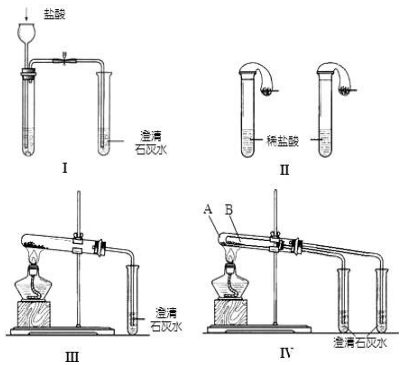
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验现象 | ⑦ | ③ | ||
| 实验结论 | ⑥ | ① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向200mL稀硫酸和稀硝酸的混合溶液中逐渐加入铁粉至过量,产生气体的量随铁粉质量增加的变化如图所示(假定硝酸只被还原为NO).则下列说法中,正确的是( )
向200mL稀硫酸和稀硝酸的混合溶液中逐渐加入铁粉至过量,产生气体的量随铁粉质量增加的变化如图所示(假定硝酸只被还原为NO).则下列说法中,正确的是( )| A. | OA段产生的是NO和H2的混合气 | B. | BC段产生的全部是NO | ||
| C. | Fe2(SO4)3是最终的溶质 | D. | H2SO4的物质的量浓度是2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
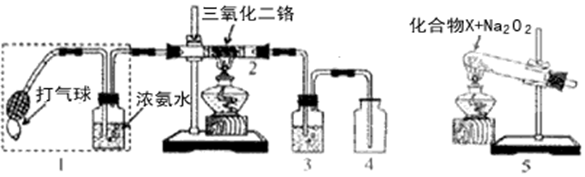
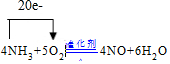 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若a≥2b,发生的反应化学方程式为:2C2H2+O2═4C+2H2O | |
| B. | 若($\frac{2}{5}$)b<a<($\frac{2}{3}$)b,燃烧后在密闭容器中加入含amolCa(OH)2的石灰水,发生反应的离子方程式为:OH-+CO2═HCO3- | |
| C. | 若a<($\frac{2}{5}$)b,燃烧过程中转移的电子的物质的量为10amol | |
| D. | 若a=($\frac{1}{2}$)b,燃烧产物既有CO2又有CO,且n(CO2):n(CO)=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、Na+、SO42-、Cl- | B. | Ba2+、Na+、OH-、SO42- | ||
| C. | OH-、HCO3-、Mg2+、Na+ | D. | K+、Na+、OH-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石和石墨互为同素异形体,熔点和硬度都很高 | |
| B. | 氕、氘、氚是氢元素的三种核素,质子数都是1 | |
| C. | 乙醇和二甲醚(CH3-O-CH3)互为同系物 | |
| D. | C4H10的一氯代物只有一种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com