
【题目】不饱和酯类化合物在药物、涂料等领域应用广泛。(6分,每空1分)
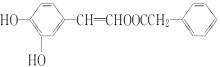
Ⅰ
(1)下列化合物Ⅰ的说法,正确的是 。
A.遇FeCl3溶液可能显紫色
B.可发生酯化反应和银镜反应
C.能与溴发生取代和加成反应
D.1 mol化合物Ⅰ最多能与2 mol NaOH反应
(2)反应①是一种由烯烃直接制备不饱和酯的新方法:
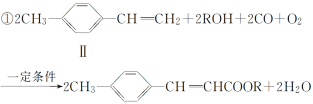
化合物Ⅱ的分子式为 ,1 mol化合物Ⅱ能与 mol H2恰好完全反应生成饱和烃类化合物。
(3)化合物Ⅱ可由芳香族化合物Ⅲ或Ⅳ分别通过消去反应获得,但只有Ⅲ能与Na反应产生H2,Ⅲ的结构简式为 (写1种);由Ⅳ生成Ⅱ的反应条件为 。
(4)聚合物![]() 可用于制备涂料,其单体结构简式为________________。
可用于制备涂料,其单体结构简式为________________。
【答案】(1)AC (2)C9H10 4
(3) 或
或![]() ;氢氧化钠醇溶液、加热
;氢氧化钠醇溶液、加热
(4)CH2=CHCOOCH2CH3
【解析】
试题分析:(1)A.该物质中含有酚羟基,能与氯化铁溶液发生显色反应,A正确;B.羟基或羧基能发生酯化反应,醛基能发生银镜反应,该物质不含醛基,不能发生银镜反应,B错误;C.酚能和溴发生取代反应、碳碳双键能和溴发生加成反应,该物质中含有酚羟基和碳碳双键,所以能发生取代反应和加成反应,C正确;D.能和NaOH反应的为酚羟基、羧基,1mol化合物I最多能与3mol NaOH反应,D错误;(2)Ⅱ中含有9个C原子、10个H原子,其化学式为C9H10;能和氢气发生加成反应的有苯环和碳碳双键,1mol化合物Ⅱ能与4mol H2恰好完全反应生成饱和烃类化合物;(3)化合物Ⅱ可由芳香族化合物Ⅲ或Ⅳ分别通过消去反应获得,但只有Ⅲ能与Na反应产生H2,说明Ⅲ中含有醇羟基,醇羟基可位于碳碳双键两端的任一个C原子上,其结构简式为 或
或![]() ;Ⅳ是卤代烃,卤代烃和氢氧化钠的醇溶液发生消去反应,所以其反应条件是氢氧化钠的醇溶液、加热;(4)聚合物
;Ⅳ是卤代烃,卤代烃和氢氧化钠的醇溶液发生消去反应,所以其反应条件是氢氧化钠的醇溶液、加热;(4)聚合物![]() 可用于制备涂料,其单体为丙烯酸乙酯,结构简式为CH2=CHCOOCH2CH3。
可用于制备涂料,其单体为丙烯酸乙酯,结构简式为CH2=CHCOOCH2CH3。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,其中每个数字编号代表对应的一种元素.
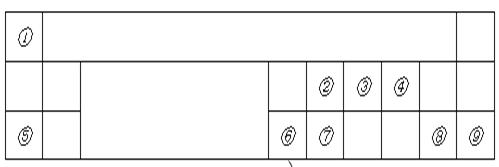
请按要求回答下列问题:
(1)画出元素②的原子结构示意图_____________________.
(2)属于稀有气体的元素编号是________________,可作半导体材料的元素编号是_________________.
(3)③、⑦两种元素相比较,非金属性强的是__________________(填元素符号).
(4)元素④的单质与元素⑤的单质反应可生成两种化合物,化学式分别是__________,______.
(5)元素③和元素⑧的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式:_________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)汽车尾气中CO、NOx以及燃煤废气中的SO2都是大气污染物,对它们的治理具有重要意义。
(1)氧化一还原法消除NOx的转化如下:
![]()
①反应I为NO +O3=NO2+O2,生成标准状况下11.2 L O2时,转移电子的物质的量是 mol。
②反应Ⅱ中,当n( NO2):n[CO(NH2)2]=3:2时,氧化产物与还原产物的质量比为______
(2)使用“催化转化器”可以减少尾气中的CO和NOx,转化过程中发生反应的化学方程式为CO+ NOx →N2+CO2(未配平),若x=1.5,则化学方程式中CO2和N2的化学计量数比为 。
(3)吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素)。装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,请写出生成等物质的量的NO3-和NO2-时的离子方程式 .

(4)装置Ⅲ的作用之一是用质子交换膜电解槽电解使得Ce4+再生,再生时生成的Ce4+在电解槽的 (填“阳极”或“阴极”),同时在另一极生成S2O42一的电极反应式为 。
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为ag.L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,至少需向装置Ⅳ中通人标准状况下的氧气 L(用含a代数式表示,结果保留整数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝基苯可在金属锡、盐酸作用下生成氯化苯铵盐(![]() )、氯化亚锡(SnCl2)和水。
)、氯化亚锡(SnCl2)和水。
(1)写出Sn2+的最外层电子排布式___________;Cl-中有_________个填充电子的能级。
(2)画出硝基的电子式____________,氯化亚锡分子的空间构型是________________;氯化苯胺盐(![]() )中N原子的杂化方式为_______________,该盐的水溶度较苯胺大的原因是____________________________________________________。
)中N原子的杂化方式为_______________,该盐的水溶度较苯胺大的原因是____________________________________________________。
(3)Sn的一种同素异形体——灰锡的晶体结构类似金刚石,立方晶胞结构如图所示,则锡的配位数是_______。
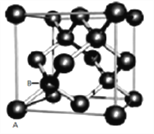
(4)假设锡原子(如图中A、B两原子)在体对角线上外切,晶胞参数为a,计算灰锡的空间利用率约为________________。(百分数表示,取两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种化合物,有的是药物,有的是香料。它们的结构简式如下所示:
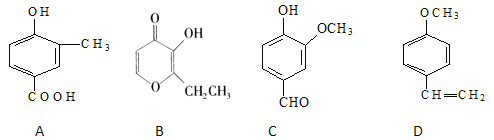
(1)化合物A的分子式是____________;C中含有的官能团的名称是_____________;
(2)A、B、C、D四种化合物中互为同分异构体的是(填序号)__________________;
(3)化合物B的核磁共振氢谱中出现_______组峰;
(4)1mol D最多能与_____________mol的氢气发生加成反应;
(5)A与乙二醇以物质的量2:1反应生成一种酯,请写出该反应的化学方程式(注明反应条件):_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂一铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O==2Cu+2Li++2OH-,下列说法不正确的是
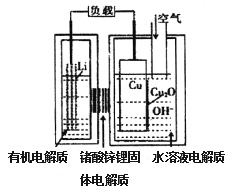
A. 放电时,正极的电极反应式为Cu2O+H2O+2e-=2OH-+2Cu
B. 放电时,电子透过固体电解质向Li极移动
C. 通空气时,铜电极被腐蚀,表面产生Cu2O
D. 整个反应过程中,氧化剂为O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.自然界中不存在游离态的硫
B.硫在空气中的燃烧产物是二氧化硫,在纯氧中的燃烧产物是三氧化硫
C.二氧化硫能使滴有酚酞的氢氧化钠溶液褪色,体现了其漂白性
D.浓硫酸可用来干燥SO2、CO、Cl2等气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烯是重要的基础有机化工原料.工业中以乙苯(C6H5-CH2CH3)为原料,采用催化脱氢的方法制取苯乙烯(C6H5-CH=CH2)的反应方程式为:C6H5-CH2CH3(g)![]() C6H5-CH=CH2(g) +H2(g)ΔH=a kJmol﹣1
C6H5-CH=CH2(g) +H2(g)ΔH=a kJmol﹣1
(1)向体积为VL的密闭容器中充入n mol乙苯,反应达到平衡状态时,平衡体系组成(物质的量分数)与温度的关系如图所示:

600℃时,该反应的平衡常数_____________。
(2)乙苯在特定催化剂下发生氧化脱氢:
C6H5-CH2CH3(g)+1/2O2(g)![]() C6H5-CH=CH2(g)+H2O(g) ΔH1
C6H5-CH=CH2(g)+H2O(g) ΔH1
已知 H2的燃烧热ΔH= b kJ/mol,水的汽化热为c J/g,则 ΔH1=____________。
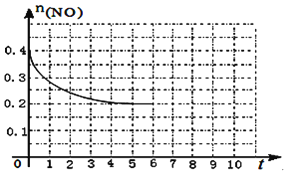
(3)在汽车上安装三元催化转化器可实现反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) △H<0。则该反应在_________ (填“高温”、“低温”或“任何温度”)下能自发进行。在某温度下,2L 密闭容器中充入NO、CO各0.4mol进行反应,测得NO物质的量变化如图所示,5分钟末反应达到平衡。第6分钟继续加入0.2 mol NO、0.2 mol CO、0.2 mol CO2和0.3 mol N2,请在图中画出到9分钟末反应达到平衡NO的物质的量随时间的变化曲线_________。
N2(g)+2CO2(g) △H<0。则该反应在_________ (填“高温”、“低温”或“任何温度”)下能自发进行。在某温度下,2L 密闭容器中充入NO、CO各0.4mol进行反应,测得NO物质的量变化如图所示,5分钟末反应达到平衡。第6分钟继续加入0.2 mol NO、0.2 mol CO、0.2 mol CO2和0.3 mol N2,请在图中画出到9分钟末反应达到平衡NO的物质的量随时间的变化曲线_________。
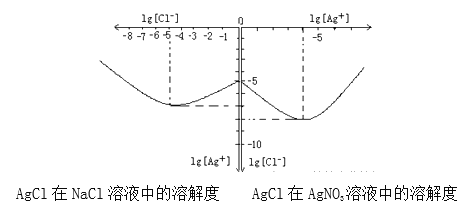
(4)沉淀物并非绝对不溶,且在水及各种不同的溶液中溶解度有所不同,同离子效应、络合物的形成等都会使沉淀物的溶解度有所改变。已知AgCl+Cl-═[AgCl2]-,如图是某温度下AgCl在NaCl溶液中的溶解情况.
由以上信息可知:
①由图知该温度下AgCl的溶度积常数为_________。
②AgCl在NaCl溶液中的溶解出现如图所示情况(先变小后变大)的原因是:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是
选项 | 混合物 | 除杂试剂 | 分离方法 |
A | 己烷(己烯) | 溴的CCl4溶液 | 分液 |
B | 溴乙烷(乙醇) | 水 | 分液 |
C | 淀粉溶液(NaCl) | 水 | 过滤 |
D | 皂化液(甘油) | NaCl | 盐析,分液 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com