
| A. | 气体单质中一定存在σ键,可能存在π键 | |
| B. | σ键可以绕键轴旋转,π键一定不能绕键轴旋转 | |
| C. | π键比σ键的电子云重叠程度大 | |
| D. | CH2=CHCl中C-Cl键采用的成键轨道是sp2-s |
分析 A.稀有气体分子中不存在化学键;
B.σ键:成键原子的电子云以“头碰头”方式重叠形成的共价键,其特征是轴对称,即以形成化学键的两原子核的连线为轴作旋转;π键:成键原子的电子云以“肩并肩”方式形成的共价键,其特征是镜像对称,不能绕键轴旋转;
C.σ键头碰头重叠,π键肩并肩重叠,σ键重叠程度大;
D.在平面形分子CH2=CHCl中,每个C原子含有3个σ键和1个π键,所以价层电子对个数是3,采用sp2杂化,Cl原子中未成对电子为3p电子,据此判断C-Cl键采用的成键轨道.
解答 解:A.稀有气体分子中不存在化学键,所以不一定存在σ键,也不一定存在π键,故A错误;
B.σ键为轴对称可以绕键轴旋转,二π键为镜像对称,一定不能绕键轴旋转,故B正确;
Cσ键头碰头重叠,π键肩并肩重叠,σ键重叠程度大,共价键强,故C错误;
D在平面形分子ClCH=CHCl中,每个C原子含有3个σ键和1个π键,所以价层电子对个数是3,采用sp2杂化,Cl原子中未成对电子为3p电子,所以C-Cl键采用的成键轨道是sp2-p,在平面形分子CH2=CHCl中,每个C原子含有3个σ键和1个π键,所以价层电子对个数是3,采用sp2杂化,Cl原子中未成对电子为3p电子,所以C-Cl键采用的成键轨道是sp2-p,故D错误;
故选:B.
点评 本题考查了有机化合物中共价键的类型,难度不大,根据单键为σ键,双键含有含有1个σ键和1个π键,σ键可以绕键轴旋转,π键不能绕键轴旋转.


 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:高中化学 来源: 题型:选择题
| A. | $\frac{{1000{ρ_1}{ρ_2}ω}}{{{ρ_1}+4}}$mol/L | B. | $\frac{{1000{ρ_1}{ρ_2}ω}}{{36.5({ρ_1}+4)}}$mol/L | ||
| C. | $\frac{{1000{ρ_1}}}{182.5}$mol/L | D. | $\frac{{1000{ρ_1}{ρ_2}ω}}{182.5}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | IA族元素的金属性比IIA族元素的金属性强 | |
| B. | 同周期非金属氧化物对应的水化物的酸性从左到右依次增强 | |
| C. | 第三周期元素的离子半径从左到右逐渐减小 | |
| D. | VIA族元素的氢化物中,稳定性最好的其沸点也最高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | Z结构中有4个手性碳原子 | |
| B. | Y的分子式为C9H8O3 | |
| C. | 1molZ余足量NaOH溶液反应,最多消耗8molNaOH | |
| D. | 1molZ与浓溴水反应最多消耗3molBr2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑦ | B. | ①⑧ | C. | ②⑧ | D. | ⑤⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 乙苯催化脱氢制苯乙烯反应:
乙苯催化脱氢制苯乙烯反应: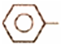 CH2CH3(g)$\stackrel{催化剂}{?}$
CH2CH3(g)$\stackrel{催化剂}{?}$ CH=CH2(g)+H2(g)
CH=CH2(g)+H2(g)| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ•molˉ1 | 412 | 348 | 612 | 436 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小 | |
| B. | 在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降 | |
| C. | 常温下pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等 | |
| D. | 0.1 mol/LC6H5ONa溶液中:c(Na+)>c(C6H5O-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com