
| ||
| ||


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:
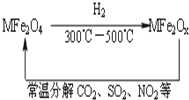 新型纳米材料氧缺位铁酸盐(MFe2Ox 3<x<4,M=Mn、Co、Zn或Ni)由铁酸盐(MFe2O4)经高温与氢气反应制得,常温下,它能使工业废气中的酸性氧化物(SO2、NO2等)转化为其单质除去,转化流程如图.关于此转化过程的叙述不正确的是( )
新型纳米材料氧缺位铁酸盐(MFe2Ox 3<x<4,M=Mn、Co、Zn或Ni)由铁酸盐(MFe2O4)经高温与氢气反应制得,常温下,它能使工业废气中的酸性氧化物(SO2、NO2等)转化为其单质除去,转化流程如图.关于此转化过程的叙述不正确的是( )| A、MFe2O4在与H2反应中表现了氧化性 |
| B、若4mol MFe2Ox与1mol SO2恰好完全反应则MFe2Ox中x的值为3.5 |
| C、MFe2Ox与SO2反应中MFe2Ox被还原 |
| D、MFe2O4与MFe2Ox的相互转化反应均属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
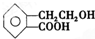 ,它可通过不同化学反应分别制得B、C、D和E四种物质.
,它可通过不同化学反应分别制得B、C、D和E四种物质.
查看答案和解析>>
科目:高中化学 来源: 题型:
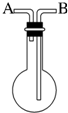 利用如图所示的装置收集以下4种气体:①NO2;②NH3;③NO;④SO2.
利用如图所示的装置收集以下4种气体:①NO2;②NH3;③NO;④SO2.查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
1 1 |
2 1 |
 和
和
查看答案和解析>>
科目:高中化学 来源: 题型:
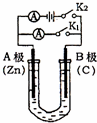 如图所示,U形管内盛有100mL的溶液,请按要求回答下列回答.
如图所示,U形管内盛有100mL的溶液,请按要求回答下列回答.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水和汽油的混合物用分液方法分离 |
| B、石灰水中悬浮的固体碳酸钙用过滤方法分离 |
| C、碘水中的碘用酒精萃取分离 |
| D、乙醇中溶解微量食盐,用蒸馏方法分离 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com