
设C+CO2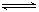 2CO △H > 0 反应速率为?1,N2+3H2
2CO △H > 0 反应速率为?1,N2+3H2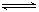 2NH3 △H<0 反应速率为?2,对于上述反应,当温度升高时,?1和?2的变化情况为
2NH3 △H<0 反应速率为?2,对于上述反应,当温度升高时,?1和?2的变化情况为
A. 同时增大 B.同时减小 C.增大,减小 D.减小,增大
科目:高中化学 来源:2014-2015学年甘肃甘谷县第一中学高一上学期第一次月考化学试卷(解析版) 题型:选择题
相等物质的量的CO和CO2的下列比较中正确的是( )
①所含的分子数目之比为1:1 ②所含的O原子数目之比为1:2
③所含的原子总数目之比为2:3 ④所含的C原子数目之比为1:1
⑤它们的质量之比为7:11
A.①② B.②③ C.④⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南长沙市高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列各组物质的性质比较中,正确的是
A.酸性:HClO4>H3PO4>H2SO4
B.氢化物的稳定性:H2S>HF>H2O
C.碱性:Al(OH)3>Mg(OH)2>NaOH
D.氧化性:F2>C12>Br2>I2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南邵阳县石齐学校高二上第一次月考化学(理)试卷(解析版) 题型:填空题
在一密闭容器中发生反应N2+3H2 2NH3 , ΔH<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
2NH3 , ΔH<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:

回答下列问题:
(1)处于平衡状态的时间段是__________(填选项)。
A t0~t1 B t1~t2 C.t2~t3
D.t3~t4 E.t4~t5 F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是(填选项),t1时刻________; t4时刻________。
A 增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是__________(填选项)。
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
(4)一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为__________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南邵阳县石齐学校高二上第一次月考化学(理)试卷(解析版) 题型:选择题
在容积不变的密闭容器中,在一定条件下发生反应:2A(?) B (g)+C(s),且达到平衡,当升高温度时,容器内气体的密度变大,则下列判断错误的是
B (g)+C(s),且达到平衡,当升高温度时,容器内气体的密度变大,则下列判断错误的是
A.若正反应为吸热反应,则A为非气态
B.若正反应为放热反应,则A为气态
C.若在平衡体系中加入少量C,则该平衡不移动
D.压强对该平衡的移动无影响
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南邵阳县石齐学校高二上第一次月考化学(理)试卷(解析版) 题型:选择题
对于任何一个平衡体系,采用以下措施,一定会使平衡移动的是
A.加入一种反应物 B.升高温度 C.对平衡体系增加压强 D.使用催化剂
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南邵阳县石齐学校高二上第一次月考化学(理)试卷(解析版) 题型:选择题
反应A(g)+B(g) 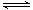 C(g)+D(g)过程中的能量变化如图所示,
C(g)+D(g)过程中的能量变化如图所示,
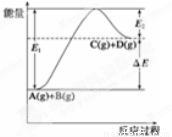
①正反应为放热反应,
②反应物总能量低于生成物总能量,
③反应物的总键能小于生成物的总键能,
④1molA与1molB充分反应后,能量变化为ΔE,
⑤加入催化剂后,反应加快,ΔE减小,
⑥反应达到平衡时,升高温度,A的转化率增大,
⑦升高温度可增大正反应速率,降低逆反应速率,
⑧E2是反应C(g)+D(g) 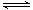 A(g)+B(g) 的活化能,
A(g)+B(g) 的活化能,
以上有关说法正确的是
A.⑤⑥⑦⑧ B.①②③④ C.①③⑤⑦ D.②⑥⑧
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省衡阳市高二上学期期中考试化学试卷(解析版) 题型:选择题
下列溶液加热蒸干灼烧后,能得到该溶质固体的是
A.Fe2(SO4)3 B.KHCO3 C.AlCl3 D.NH4NO3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列有关物质的性质和应用均正确的是( )
①氯气具有酸性,可与烧碱或石灰乳反应制备含氯消毒剂,84消毒液的有效成分是NaClO
②浓硫酸具有强氧化性,不能干燥SO2等还原性的气体;过氧化钠具有强氧化性,可用作潜水艇中氧气的来源
③硅在元素周期表中处于金属与非金属的交界位置,是重要的半导体材料,在自然界中可以以游离态和化合态的形式存在
④浓氨水可检验氯气管道是否漏气
⑤玻璃容器可长期盛放各种酸
⑥Na2S可除去污水中的Cu2+
⑦碘酒是指单质碘的乙醇溶液
⑧明矾作净水剂,液氨用作制冷剂,生石灰作干燥剂
A.①④⑦⑧ B.④⑥⑦⑧ C.②⑦⑧ D.②③⑦⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com