
| A、测得0.1 mol?L-1氨水的pH为11:NH3?H2O?NH4++OH- | ||||
| B、将Na块投入水中,产生气体:2Na+2H2O═2NaOH+H2↑ | ||||
C、用CuCl2溶液做导电实验,灯泡发光:CuCl2
| ||||
D、将1 mol?L-1FeCl3溶液滴入沸水中,得到透明红褐色液体:FeCl3+3H2O
|
| ||


科目:高中化学 来源: 题型:
| A、0.25mol |
| B、0.2mol |
| C、0.15mol |
| D、0.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
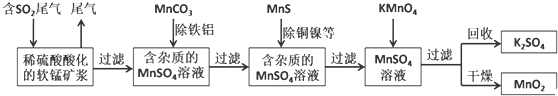
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、光导纤维和陶瓷都是硅酸盐产品 |
| B、晶体硅可用于制造芯片 |
| C、钢铁厂用热还原法冶炼铁 |
| D、焙制糕点的发酵粉主要成分之一是碳酸氢钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 现象 | 结论 |
| A | SO2通入溴水中 | 溶液褪色 | SO2有漂白性 |
| B | 将Fe(NO3)2样品溶于稀H2SO4,滴加KSCN溶液 | 溶液变红 | Fe(NO3)2样品已氧化变质 |
| C | 将新制氯水和KI溶液在试管中混合后,加入CCl4,振荡静置 | 溶液分层,下层呈紫色 | 氧化性:Cl2>I2 |
| D | 分别向0.1 mol?L-1醋酸和饱和硼酸溶液中滴加0.1mol?L-1Na2CO3溶液 | 醋酸中有气泡产生,硼酸中没有气泡产生 | 酸性:醋酸>碳酸>硼酸 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
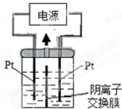
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2H2(g)+O2(g)=2H2O (l)△H=-285.8 kJ?mol-1 |
| B、2H2(g)+O2(g)=2H2O (l)△H=+571.6 kJ?mol-1 |
| C、2H2(g)+O2(g)=2H2O (g)△H=-571.6 kJ?mol-1 |
| D、H2(g)+1/2O2(g)=H2O (l)△H=-285.8 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ①443-573K |
| 熔烧 |
| ②进一步加热 |
| 到773-873K |
| 通入水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 开始沉淀的pH | 完全沉淀的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |

| KMnO4(OH-)溶液 | 铁钉(钢钉) | |
| 实验1 | 短时间内无明显现象 | 短时间内无明显现象 |
| 实验2 | 短时间溶液由紫红色(MnO4-)变为深绿色(MnO42-) | 短时间铁钉表面产生红褐色物质 |
| 请用化学用语解释实验2的现象 | | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com