
【题目】已知A为某种聚甲基丙烯酸酯纤维(M)的单体,其转化关系如图:

回答下列问题:
(1)B中含氧官能团的结构简式为_______;C用系统命名法命名为___________________。
(2)反应A→M的反应类型为___________;M的结构简式为___________________________。
(3)反应C→D的化学方程式为_______________________________。F与银氨溶液反应的化学方程式为________________________。
(4)关于E的下列说法正确的是________________(填写序号)。
①分子中所有碳原子都在同一平面上;
②能与H2反应;
③能与NaOH的醇溶液反应;
④能与溴水反应。
(5)写出满足下列条件的A的同分异构体的结构简式:______________________。
①与A具有相同的官能团;
②水解产物之一(相对分子质量为108)遇FeCl3溶液显紫色;
③核磁共振氢谱有5种峰。
【答案】—COOH 2-甲基丙酸 加聚反应  (CH3)2CHCOOH+CH3CH2OH
(CH3)2CHCOOH+CH3CH2OH![]() (CH3)2CHCOOCH2CH3+H2O
(CH3)2CHCOOCH2CH3+H2O ![]() +2Ag(NH3)2OH
+2Ag(NH3)2OH![]()
![]() +2Ag↓+3NH3+H2O ①②④
+2Ag↓+3NH3+H2O ①②④ 
【解析】
A为某种聚甲基丙烯酸酯纤维(M)的单体,A在酸催化剂条件下水解生成B与E,A含有酯基,B连续发生氧化反应生成苯甲酸,则E为![]() ,F为
,F为![]() ,结合A的分子式可知B的分子式为C4H6O2,B含有羧基,不饱和度为2,结合A可以形成高聚物M,可知B还含有1个碳碳双键,结合M的名称可知B中含有甲基,则B为CH2=C(CH3)COOH,B与氢气发生加成反应生成C为(CH3)2CHCOOH,C与乙醇发生酯化反应生成D为(CH3)2CHCOOCH2CH3,故A为
,结合A的分子式可知B的分子式为C4H6O2,B含有羧基,不饱和度为2,结合A可以形成高聚物M,可知B还含有1个碳碳双键,结合M的名称可知B中含有甲基,则B为CH2=C(CH3)COOH,B与氢气发生加成反应生成C为(CH3)2CHCOOH,C与乙醇发生酯化反应生成D为(CH3)2CHCOOCH2CH3,故A为 ,M为
,M为 ,据此解答。
,据此解答。
(1)由以上推断可知,B为CH2=C(CH3)COOH,含有官能团有:碳碳双键、羧基,结构简式分别为:![]() 、-COOH,C为(CH3)2CHCOOH,名称为:2-甲基丙酸;
、-COOH,C为(CH3)2CHCOOH,名称为:2-甲基丙酸;
(2)反应A→M是 发生加聚反应生成高聚物M,M的结构简式为
发生加聚反应生成高聚物M,M的结构简式为 ;
;
(3)①反应C→D的化学方程式为:(CH3)2CHCOOH+CH3CH2OH![]() (CH3)2CHCOOCH2CH3+H2O,
(CH3)2CHCOOCH2CH3+H2O,
②F与银氨溶液反应的离子方程式为:![]() +2Ag(NH3)2OH
+2Ag(NH3)2OH![]()
![]() +2Ag↓+3NH3+H2O,
+2Ag↓+3NH3+H2O,
(4)E为![]() ,
,
①分子存在苯环平面计算,所有碳原子都处于苯环平面内,故正确;
②含有苯环,能与H2反应发生加成反应,故正确;
③羟基相邻的相邻碳原子上没有H原子,不能能与NaOH醇溶液反应,故错误;
④含有醇羟基,能与HBr发生取代反应,故正确,
故选:①②④;
(5)满足下列条件的A( )的同分异构体的结构简式:①与A具有相同的官能团 ②水解产物之一(式量为108)遇FeCl3溶液显紫色,该产物为甲基苯酚,③核磁共振氢谱有5种峰,符合条件的同分异构体为
)的同分异构体的结构简式:①与A具有相同的官能团 ②水解产物之一(式量为108)遇FeCl3溶液显紫色,该产物为甲基苯酚,③核磁共振氢谱有5种峰,符合条件的同分异构体为 。
。


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案科目:高中化学 来源: 题型:
【题目】请完成下列填空:
(1)当SO2和SO3中分子个数比为1:1 时,原子总数之比为____,质量之比为____。
(2)将5mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度是______。
(3)中和含0.2molHCl的稀盐酸,需NaOH的物质的量为_______;如改用KOH,则所需KOH的质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现代人追求“低碳生活” ,二氧化碳的回收并利用是环保领域研究的热点和重点。试分析并回答:
(1)有一最新美国科学家的研究成果,利用金属钛和某些装置等,模仿太阳的蓝色波长,使CO2慢慢发生人工“光合作用” 后,被还原成太阳能燃料——甲酸等,该化学方程式是_____________________________;
(2)另有一种用CO2生产甲醇燃料的方法:
CO2+3H2=CH3OH+H2O。已知298 K和101 kPa条件下:
CO2(g)+3H2(g)=CH3OH(g)+H2O(l) ΔH=-a kJ·mol-1;
2H2(g)+O2(g)=2H2O(l) ΔH=-b kJ·mol-1;
CH3OH(g)=CH3OH(l) ΔH=-c kJ·mol-1,
则CH3OH(l)的标准燃烧热ΔH=________。
(3)工业上合成尿素的反应如下:
2NH3(g)+CO2(g)=CO(NH2)2(l)+H2O(l) ΔH<0,某实验小组模拟工业上合成尿素的条件,在恒定温度下,将氨气和二氧化碳按2∶1的物质的量之比充入一体积为10 L的密闭容器中(假设容器体积不变,生成物的体积忽略不计),经20 min达到平衡,各物质浓度的变化曲线如图所示。
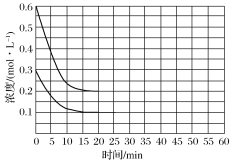
①为提高尿素的产率,下列可以采取的措施有________;
A.缩小反应容器的容积
B.升高温度
C.平衡体系中分离出部分CO(NH2)2
D.使用合适的催化剂
②若保持平衡的温度和压强不变,再向容器中充入3 mol的氨气,则此时v正________v逆(填“>”“=”或“<”),判断理由_____________________________;
③若保持平衡的温度和体积不变,25 min时再向容器中充入2 mol氨气和1 mol二氧化碳,在40 min时重新达到平衡,请在上图中画出25~50 min内氨气的浓度变化曲线________________。
(4)多孔Al2O3薄膜可作为催化剂载体、模板合成纳米材料等用途。现以高纯铝片作为阳极,不锈钢作为阴极,一定溶度的磷酸溶液作为电解质进行电解,即可初步制取多孔Al2O3膜。请写出该制取过程的阳极电极反应:__________________________________________。
(5)要实现CO2直接加H2合成汽油,关键是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式不正确的是( )
A.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3(胶体)+3H+
Fe(OH)3(胶体)+3H+
B.用小苏打治疗胃酸过多:CO32-+2H+=CO2↑+H2O
C.实验室用浓盐酸与MnO2制备氯气:MnO2+4H++2Cl-![]() Mn2++2H2O+Cl2↑
Mn2++2H2O+Cl2↑
D.过氧化钠与水反应:2Na2O2+2H2O=4OH-+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液X,由Na+、Mg2+、Ba2+、Al3+、AlO2-、MnO![]() 、CO
、CO![]() 、SO
、SO![]() 中的若干种离子组成,取溶液进行如下连续实验:
中的若干种离子组成,取溶液进行如下连续实验:
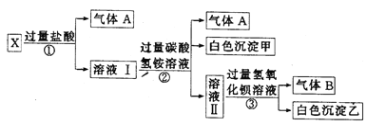
(1)气体A的成分是_______(填电子式),气体B的成分是_______(填结构式)
(2)X溶液中一定不存在的离子是______________。
(3)写出步骤①中发生反应的所有离子方程式:________________。
(4)写出步骤②中形成白色沉淀的离子方程式:________________。
(5)通过上述实验,溶液X中不能确定是否存在的离子是______________;只要设计一个简单的后续实验就可以确定该离子是否存在,该方法是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L的恒容密闭容器中充入![]() 和
和![]() ,发生反应
,发生反应![]()
![]() ,实验内容和结果分别如表和图所示,下列说法不正确的是( )
,实验内容和结果分别如表和图所示,下列说法不正确的是( )

实验序号 | 温度 | 起始物质的量 | 热量变化 | |
A | B | |||
I |
| 1mol | 3mol | 96kJ |
II |
|
|
| |
A.实验Ⅰ中,10min内平均速率![]()
![]()
B.上述方程式中![]()
C.![]() 时,该反应的平衡常数是
时,该反应的平衡常数是![]()
D.向实验Ⅱ的平衡体系中再充入![]() molA和
molA和![]() molB,A的转化率增大
molB,A的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用勒沙特列原理解释的是( )
A.500℃左右比室温更有利于合成氨的反应
B.低压有利于合成氨的反应
C.SO2催化氧化成SO3的反应,往往需要使用催化剂
D.实验室常用排饱和食盐水的方法收集氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲配制480mL0.5mol·L-1的CuSO4溶液,据此回答下列问题:
(1)需称量胆矾CuSO4.5H2O__g。
(2)在配制的过程中一定不需要使用到的仪器是(填写代号)__,还缺少的仪器有__、__。
A.烧杯 B.药匙 C.玻璃棒 D.1000mL容量瓶 E.锥形瓶 F.胶头滴管
(3)如图所示的实验操作的先后顺序为__。
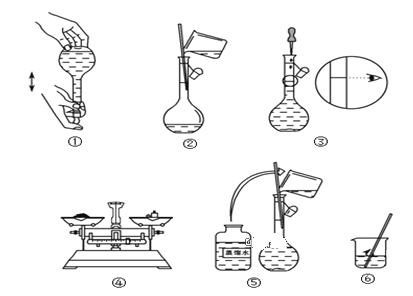
(4)从配制好的CuSO4溶液中取出10mL,将这10mL的CuSO4溶液稀释至100mL,稀释后CuSO4溶液的浓度变为__mol·L-1。
(5)下列的实验操作可能导致配制的溶液浓度偏低的是__。
A.容量瓶内原来存有少量的水
B.定容时液面超过刻度线,用胶头滴管吸出
C.称量所需CuSO4.5H2O的质量时,物品与砝码的位置放反了(1g以下用游码)
D.定容时俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M是有机合成的重要中间体,制备M的一种合成路线如下(部分反应条件和试剂已略去)
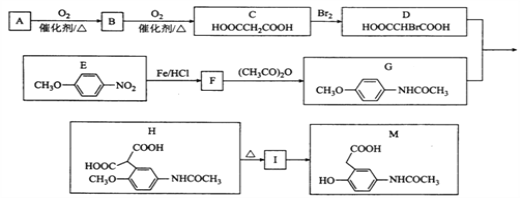
已知: ①A的密度是相同条件下H2密度的38倍;其分子的核磁共振氢谱中有3组峰;
②![]()
③![]()
请回答下列问题:
(1)B的化学名称为______________。A中官能团的电子式为________________。
(2)C中共面的原子最多有________个。I的结构简式为_____________________。
(3)F→G的化学方程式为________________________________________________。
(4)M不可能发生的反应为_______________(填选项字母)
A.加成反应 B.氧化反应 C.取代反应 D.消去反应
(5)同时满足下列条件的E的同分异构体有_________种。
①能与FeCl3溶液发生显色反应 ②能与NaHCO3反应 ③含有—个—NH2
(6)参照上述合成路线,以 ![]() 为原料(无机试剂任选),设计制备
为原料(无机试剂任选),设计制备![]() 的合成路线:_______________________________________________。
的合成路线:_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com