
���� ��1������Ȧ�=$\frac{�ѵ���Ĵ������}{�����������}$��100%��CH3COOH�ĵ���ƽ�ⳣ��Ka=$\frac{c��{H}^{+}��c��C{H}_{3}CO{O}^{-}��}{c��C{H}_{3}COOH��}$�ݴ˼��㣻
��2��Na2A��Һ��pH=7��˵��Na2A��ˮ�⣬��H2AΪǿ��ȼ���ϡ�ͺ���Һ��������Ũ�ȣ�����PH��
��3�����ø�˹���ɽ��м��㣬�ֱ�д��������Ӧ���Ȼ�ѧ����ʽ���������Ȼ�ѧ����ʽ��ӣ������õ�HCN��ˮ��Һ�е���ĵ��뷽��ʽ��ͬʱ��Ӧ��Ҳ��֮��ӣ��������ɵ�HCN��ˮ��Һ�е���ķ�Ӧ�ȣ�
��4����ƽ�ⳣ��=$\frac{������ƽ������ݴη��˻�}{��Ӧ��ƽ������ݴη��˻�}$��
�ڽ�ϻ�ѧƽ������ʽ��ʽ���㣬����ѹǿ֮�ȵ����������ʵ���֮�ȼ���õ���
��� �⣺��1����CH3COOH?CH3COO-+H+֪��c��H+�������Ѿ������c��CH3COOH���������Ѿ�����Ĵ���Ũ����1.0��10-3mol/L��
���Ԧ�=$\frac{�ѵ���Ĵ������}{�����������}$��100%=$\frac{1��1{0}^{-3}mol/L}{0.1mol/L}$��100%=1%����CH3COOH?CH3COO-+H+֪��c��H+��=c��CH3COO-��=�Ѿ������c��CH3COOH������Һ��δ����Ĵ���Ũ��Ϊ��0.1-0.001��mol/L��Ka=$\frac{c��{H}^{+}��c��C{H}_{3}CO{O}^{-}��}{c��C{H}_{3}COOH��}$=$\frac{0.001��0.001}{0.1}$=10-5��
�ʴ�Ϊ��1%��10-5��
��2����25��ʱ��Kw=1.0��10-14�����¶��´�ˮ��pH=7�����0.1mol•L-1 Na2A��Һ��pH=7��˵��Na2A��ǿ��ǿ���Σ�
H2A��ǿ�ᣬ��ˮ��Һ����ȫ���룬����뷽��ʽΪH2A�T2H++A2-�����¶��£���0.01mol•L-1 H2A��Һϡ�͵�20������Һ��������Ũ��=0.01mol/L��2��20=0.001mol/L������pH=3��
�ʴ�Ϊ��H2A�T2H++A2-��3��
��3����Ӧ���Ȼ�ѧ����ʽ�ֱ�Ϊ��
HCN��aq��+OH-��aq���TCN-��aq��+H2O��l����H=-12.1kJ•mol-1����
H+��aq��+OH-��aq���TH2O��l����H=-57.3kJ•mol-1����
HCN���뷽��ʽΪ��HCN?H++CN-���â�-�ڿɵ�HCN������Ȼ�ѧ����ʽΪ��
HCN��aq��?H+��aq��+CN-��aq����H=-12.1kJ•mol-1-��-57.3kJ•mol-1��=+45.2kJ•mol-1��
�ʴ�Ϊ��+45.2��
��4��CO2��g��+3H2��g��=CH2OH��g��+H2O��g��
���������淴Ӧ��ƽ�ⳣ������ʽK=$\frac{������ƽ������ݴη��˻�}{��Ӧ��ƽ������ݴη��˻�}$=$\frac{c��C{H}_{3}OH��c��{H}_{2}O��}{c��C{O}_{2}��{c}^{3}��{H}_{2}��}$��
�ʴ�Ϊ��$\frac{c��C{H}_{3}OH��c��{H}_{2}O��}{c��C{O}_{2}��{c}^{3}��{H}_{2}��}$��
����T1��ʱ����1molCO2��3molH2����һ�ܱպ��������У���ַ�Ӧ�ﵽƽ�����CO2��ת����Ϊa��
CO2��g��+3H2��g��=CH2OH��g��+H2O��g��
��ʼ����mol�� 1 3 0 0
�仯����mol�� a 3a a a
ƽ������mol�� 1-a 3-3a a a
�����ڵ�ѹǿ����ʼѹǿ֮��=��4-2a����4=$\frac{1-a}{2}$��
�ʴ�Ϊ��$\frac{1-a}{2}$��
���� ���⿼����������ʵĵ���ƽ�⡢����Ⱥ͵��볣���ļ��㡢��˹���ɵ�Ӧ�á���ѧƽ������֪ʶ�㣬��ȷ������ʵ���ƽ���ص㼰�йؼ��㹫ʽ�ǽⱾ��ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | MnO2 | B�� | KMnO4 | C�� | NaClO | D�� | KClO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
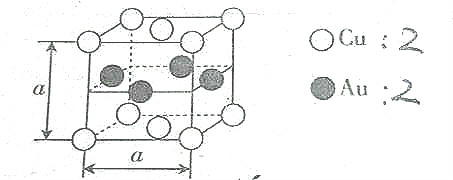
| A�� | �úϽ��������Ӿ��� | B�� | �úϽ���Au����λ����4 | ||
| C�� | �úϽ���Cu����λ����8�� | D�� | �úϽ��Ӳ�ȵ���Cu |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
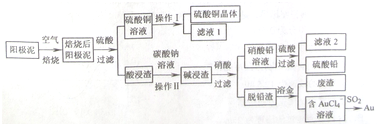
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 | V��0.5mol•L-1 HCl��/mL | m��CaCO3��/g | CaCO3״̬ | V������ˮ��/mL | ʵ��Ŀ�� | |
| ʵ��1 | 40.0 | 0.8 | ��ʵ��1��2̽�����������Է�Ӧ���ʵ�Ӱ�죻 ��ʵ��1��3̽����Ӧ��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�� | |||
| ʵ��2 | 40.0 | 0.8 | ||||
| ʵ��3 | 60.0 | 0.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ | B�� | ֻ�Тٲ��ܷ��� | C�� | ֻ�Тڲ��ܷ��� | D�� | ֻ�Т٢ܲ��ܷ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������X��Y�����ʵ���Ũ��֮������1��2ʱ����Ӧ�ﵽƽ�� | |
| B�� | �ﵽƽ���Ӧ����3v����Y��=2v�棨z�� | |
| C�� | �ﵽƽ��ʱ��X��ת����Ϊ25%����ƽ�ⳣ��KֵΪ$\frac{1}{16}$ | |
| D�� | �ﵽƽ��������¶ȣ�X������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
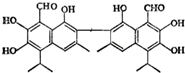 �������̨�������������������۵�ijƷ�Ƽ���Ϊ����Ƥ���������������ʤ��ƹ���������Ϊ�漦����ר�ҽ��ܣ��������ڼ����������������ѱ����Ӷ�ʹ�����ﺬ�й��������£���ṹ��ʽ��ͼ��ʾ������˵������ȷ���ǣ�������
�������̨�������������������۵�ijƷ�Ƽ���Ϊ����Ƥ���������������ʤ��ƹ���������Ϊ�漦����ר�ҽ��ܣ��������ڼ����������������ѱ����Ӷ�ʹ�����ﺬ�й��������£���ṹ��ʽ��ͼ��ʾ������˵������ȷ���ǣ�������| A�� | �û�����ķ���ʽΪ��C30H30O8 | |
| B�� | 1mol��������10mol H2�ӳɣ���6molNaOH��Ӧ | |
| C�� | ��һ�������£��������ᷴӦ������������ | |
| D�� | �����ʿ���ʹ���Ը��������Һ��ɫ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com