
关于氢键,下列说法正确的是
A.由于冰中的水分子间存在氢键,所以其密度大于液态水
B.可以用氢键解释接近沸点的水蒸气的相对分子质量测定值比用化学式(H2O)计算出来的相对分子质量大
C.分子间氢键和分子内氢键都会使熔沸点升高
D.水加热到很高的温度都难以分解,这是由于氢键所致
科目:高中化学 来源: 题型:
用惰性电极分别电解下列各物质的水溶液,一段时间后,向剩余电解质溶液中加入适量水能使溶液恢复到电解前的浓度的是( )
A.AgNO3 B.Na2SO4
C.CuCl2 D.HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室里需要纯净的溶液,但现在只有混有硫酸钠、碳酸氢铵的氯化钠。某学生设计了如下方案:
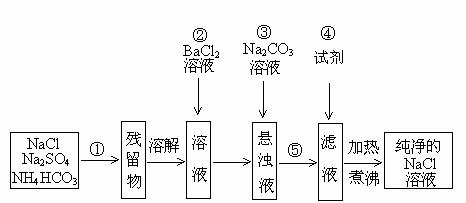 |
根据以上设计方案,回答下列问题:
(1)操作①和⑤的方法分别是 、 ;
(2)操作②是否可改为加硝酸钡溶液?为什么?
,(填是或否)理由: 。
(3)操作②后,如何判断SO42-已除尽,方法是
。
(4)操作③的目的是 ;
(5)操作④加的试剂是 ;发生反应的离子方程式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氯化铝易溶于苯和乙醚,其熔点为190℃,则下列结论正确的是
A.氯化铝硬度大,固体可导电
B.氯化铝易溶于有机溶剂,难溶于水
C.氯化铝中存在离子键
D.氯化铝属于分子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
现有三种元素的基态原子的电子排布式如下:① [Ne]3s23p4;② 1s22s22p63s23p3;③1s22s22p5。则上述三种原子的第一电离能大小关系正确的是
A.②>①>③ B.③>①>②
C.③>②>① D.①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
2.0 mol PCl3和1.0 mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g) PCl5(g) 达平衡时PCl5为0.40 mol,如果此时再加入2.0 mol PCl3和1.0 mol Cl2,在相同温度下再达平衡时PCl5的物质的量是
PCl5(g) 达平衡时PCl5为0.40 mol,如果此时再加入2.0 mol PCl3和1.0 mol Cl2,在相同温度下再达平衡时PCl5的物质的量是
A.小于0.40 mol B.大于0.80 mol
C.等于0.80 mol D.大于0.40 mol,小于0.80 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
只用一种试剂区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3、(NH4)2SO4五种溶液, 这种试剂是( )
A.Ba(OH)2 B.H2SO4 C.NaOH D.AgNO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com