
【题目】黑色冶金工业中除了铁、锰、铬、钒、钛以及这些金属的黑色金属合金以外,其他的金属,都算是有色金属。
![]() 基态钛原子的结构示意图为________;基态铬原子的价层电子排布式为________。
基态钛原子的结构示意图为________;基态铬原子的价层电子排布式为________。
![]() 中C、N的电负性关系为C________
中C、N的电负性关系为C________![]() 填“
填“![]() ”或“
”或“![]() ”
”![]() ;
;![]() 的沸点比
的沸点比![]() 的沸点低,其原因是________。
的沸点低,其原因是________。
![]() 中C原子的杂化方式为________;
中C原子的杂化方式为________;![]() 分子是________
分子是________![]() 填“极性”或“非极性”
填“极性”或“非极性”![]() 分子;
分子;![]() 分子中
分子中![]() 键与
键与![]() 键的数目之比为________。
键的数目之比为________。
![]() 金属锰的一种晶体为面心立方最密堆积,其晶胞中有________个锰原子,每个锰原子周围紧邻的锰原子有________个。
金属锰的一种晶体为面心立方最密堆积,其晶胞中有________个锰原子,每个锰原子周围紧邻的锰原子有________个。
![]() 因
因![]() 和
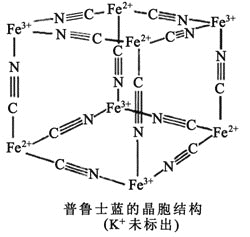
和![]() 外围有较多能量相近的空轨道,故能与一些分子或离子形成配合物。如图为普鲁士蓝配合物晶体结构的示意图
外围有较多能量相近的空轨道,故能与一些分子或离子形成配合物。如图为普鲁士蓝配合物晶体结构的示意图![]() 每两个立方体中,一个
每两个立方体中,一个![]() 在其中一个立方体中心,另一个则无
在其中一个立方体中心,另一个则无![]() ,其化学式是________。
,其化学式是________。
【答案】
![]()
![]()
![]() 分子间可形成氢键
分子间可形成氢键 ![]() 非极性
非极性 ![]()
![]() 12
12 ![]()
【解析】
(1)钛的原子序数为22,所以其原子结构示意图为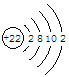 ;根据构造原理、洪特规则可知基态铬原子的价层电子排布式为
;根据构造原理、洪特规则可知基态铬原子的价层电子排布式为![]() ;
;
故答案为: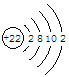 ;
;![]() ;
;
(2)根据同周期元素电负性的递变规律可知氮的电负性大于碳的电负性;由于氨分子间存在氢键,所以氨分子的沸点高于甲烷;
故答案为:![]() ;
;![]() 分子间可形成氢键;
分子间可形成氢键;
(3)根据等电子体原理分析可知![]() 中的碳原子形成了一个σ键,有一对孤电子对,所以碳原子的杂化方式为sp杂化;根据氰分子的结构
中的碳原子形成了一个σ键,有一对孤电子对,所以碳原子的杂化方式为sp杂化;根据氰分子的结构![]() 可知该分子结构对称,正负电荷中心重合,为非极性分子;根据氰分子的结构
可知该分子结构对称,正负电荷中心重合,为非极性分子;根据氰分子的结构![]() 可知
可知![]() 分子中
分子中![]() 键与
键与![]() 键的数目之比为3:4;
键的数目之比为3:4;
故答案为:sp;非极性;3:4;
(4)由于金属锰的一种晶体为面心立方最密堆积,所以晶胞中锰原子的个数为:![]() ;根据锰的晶胞结构可知每个面上与锰原子紧邻的锰原子有4个,所以与其紧邻的锰原子共有:
;根据锰的晶胞结构可知每个面上与锰原子紧邻的锰原子有4个,所以与其紧邻的锰原子共有:![]() 个;
个;
故答案为:4;12;
(5)根据给定的结构分析可知![]() 个数为:
个数为:![]() ,
,![]() 个数为:
个数为:![]() ,
,![]() 个数为:
个数为:![]() ,根据电荷守恒可知钾离子个数为:
,根据电荷守恒可知钾离子个数为:![]() ,所以晶体的化学式为
,所以晶体的化学式为![]() ;
;
故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:
(1)NH3的电子式______。
(2)氯化铵水溶液显酸性,其原因为______(用离子方程式表示),0.1mol/L的氨水中加入少量的NH4Cl固体,溶液的pH______(填“升高”或“降低”);若加入少量的明矾固体后,请尝试从平衡移动的角度解释溶液中NH4+浓度的变化原因______。
(3)硝酸铵加热分解可得到N2O(g)和H2O(g),250℃时,硝酸铵在密闭容器中分解达到平衡,该温度下反应的平衡常数表达式为______;若有1mol硝酸铵完全分解,转移的电子数为______mol。
(4)3H2(g)+N2(g)2NH3(g)△H=-92kJ/mol,若反应放出9.2kJ 热量,则参加反应的氢气分子数目为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为![]() 的密闭容器内,物质D在
的密闭容器内,物质D在![]() 时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述不正确的是
时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述不正确的是
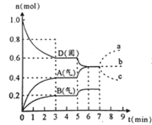
A.从反应开始到第一次达到平衡时,B物质的平均反应速率为![]()
B.该反应的化学方程式为![]() ,该反应的平衡常数表达式为
,该反应的平衡常数表达式为![]()
C.已知:反应的![]() ,则第5分钟时图象呈现上述变化的原因可能是升高体系的温度
,则第5分钟时图象呈现上述变化的原因可能是升高体系的温度
D.若在第7分钟时增加D的物质的量,则表示A的物质的量变化正确的是b曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香草酸广泛用于食品调味剂, 作香精、 香料, 合成线路如下:
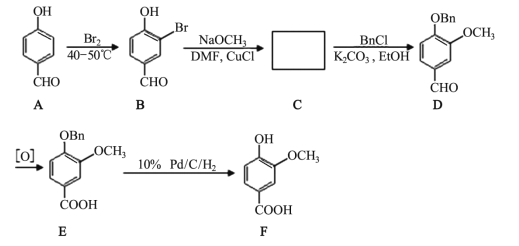
(1)C 的结构简式是_____, B 转化为 C 的反应类型为_____。
(2)A 中含有的官能团名称是_____。
(3)B 的分子式是_____。
(4)在 B 中滴入 FeCl3溶液, 其现象是_____。
(5)与 F 官能团相同的芳香族化合物的同分异构体有_____种。
(6)写出 F 与乙醇进行酯化反应的方程式_____。
(7)写出由 的合成线路图_____。
的合成线路图_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某一容积为2L的密闭容器内,加入0.8mol的H2和0.6mol的I2,在一定的条件下发生如下反应:H2(g)+I2(g)![]() 2HI(g)ΔH=-QkJ/mol(Q>0),反应中各物质的浓度随时间变化情况如图1:
2HI(g)ΔH=-QkJ/mol(Q>0),反应中各物质的浓度随时间变化情况如图1:
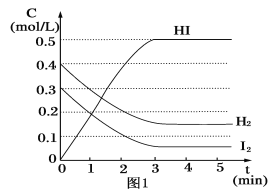
(1)该反应的化学平衡常数表达式为__。
(2)根据图1数据,反应开始至达到平衡时,平均速率v(HI)为__。
(3)反应达到平衡后,第8分钟时:
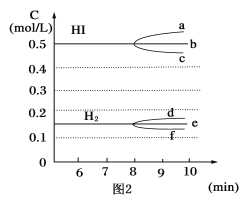
①若升高温度,化学平衡常数K__(填写增大、减小或不变)。HI浓度的变化正确的是__(用图2中a~c的编号回答)。
②若加入I2,H2浓度的变化正确的是__(用图2中d~f的编号回答)。
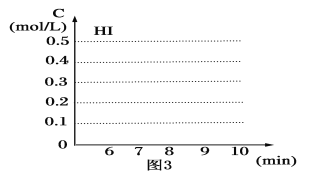
(4)反应达到平衡后,第8分钟时,若把容器的容积扩大一倍,请在图3中画出8分钟后HI浓度的变化情况___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图。
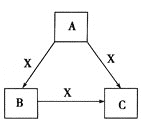
请针对以下三种不同情况回答:
![]() 若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀。
若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀。
![]() 中含有的金属元素在元素周期表中的位置为_______________________,向水中加入X物质,X对水的电离平衡的影响是_________
中含有的金属元素在元素周期表中的位置为_______________________,向水中加入X物质,X对水的电离平衡的影响是_________![]() 填“促进”、“抑制”或“无影响”
填“促进”、“抑制”或“无影响”![]() 。
。
![]() 与C的水溶液混合后生成B,反应的离子方程式为___________________________。
与C的水溶液混合后生成B,反应的离子方程式为___________________________。
![]() 若A为固态非金属单质,A与X同周期,同时A在X中燃烧,生成
若A为固态非金属单质,A与X同周期,同时A在X中燃烧,生成![]() 和
和![]() 白色烟雾,常温常压下C为白色固体,B分子中各原子最外层均为8电子结构。
白色烟雾,常温常压下C为白色固体,B分子中各原子最外层均为8电子结构。
![]() 若A为该元素的白色固体单质,其结构为正四面体,分子式为
若A为该元素的白色固体单质,其结构为正四面体,分子式为![]() ,则
,则![]() 单质中含共价键数目为_________
单质中含共价键数目为_________![]() ,B的电子式为_________。
,B的电子式为_________。
![]() 与水反应的离子方程式为_______________________________________________。
与水反应的离子方程式为_______________________________________________。
![]() 若A、B、C的焰色反应呈黄色,A为淡黄色固体,B、C的水溶液均为碱性,A溶于水后可与X反应生成C,常温下,X为气态酸性氧化物。
若A、B、C的焰色反应呈黄色,A为淡黄色固体,B、C的水溶液均为碱性,A溶于水后可与X反应生成C,常温下,X为气态酸性氧化物。
![]() 中所含有的化学键类型是_________。
中所含有的化学键类型是_________。
![]() 溶液中离子浓度由小到大的顺序是_________。
溶液中离子浓度由小到大的顺序是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了制备氯气,某同学查阅资料发现实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)请用双线桥法对该反应进行标注_________________________________。
(2)写出该反应的离子方程式________________。
(3)该同学用43.5g MnO2与足量的 HCl(浓)反应,可制备标况下的氯气的体积为_______ L,反应中转移的电子的物质的量为_______mol,反应中被氧化的HCl物质的量为_______mol。
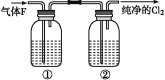
(4)在实验室中,欲用如图中的装置净化氯气,则瓶①②中应盛放的试剂分别是①____,②_____(填试剂名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如图所示。下列说法不正确的是( )

A.盐酸的浓度越大,腐蚀速率越快
B.碳素钢的腐蚀速率不随硫酸的浓度增大而增大,说明反应速率不与c(H+)成正比
C.钼酸钠和月桂酰肌氨酸的浓度相等时,腐蚀速率最小
D.对比盐酸和硫酸两条曲线,可知Cl-也可能会影响碳素钢的腐蚀速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】S16O2与18O2在高温条件下发生反应2SO2+O2![]() 2SO3,达到化学平衡后,平衡混合物中含18O的微粒( )
2SO3,达到化学平衡后,平衡混合物中含18O的微粒( )
A. 只有SO3 B. 只有SO2、SO3 C. 有SO2、SO3、O2 D. 只有O2、SO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com