
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率,属于牺牲阴极的阳极保护法 | |
| C. | 根据分散质粒子的大小分类,将分散系分为溶液、浊液、胶体 | |
| D. | 为防止月饼等富脂等食品被氧化,常在包装中放入还原铁粉等 |
分析 A.Al(OH)3胶体具有较大的表面积,有吸附性;
B.Zn与Fe形成原电池时,Fe作正极被保护;
C.根据分散系中分散质粒子直径大小分类;
D.为了防止中秋月饼的富脂食物因被氧化而变质,应加入还原性物质.
解答 解:A.明矾在水中电离的铝离子能水解生成Al(OH)3胶体,Al(OH)3胶体具有较大的表面积,有吸附性,能吸附水中的悬浮物,可用于水的净化,故A错误;
B.Zn与Fe形成原电池时,Zn的活泼性比Fe强,Fe作正极被保护,所以在海轮外壳上镶入锌块,可减缓船体的腐蚀速率,故B正确;
C.根据分散系中分散质粒子直径大小将分散系分为溶液、胶体和浊液,故C错误;
D.铁粉具有还原性,能防止中秋月饼的富脂食物因被氧化而变质,故D错误.
故选B.
点评 本题考查了胶体性质的应用、原电池原理的应用、分散系、食品添加剂等,题目难度不大,侧重于基础知识的考查,注意对有关原理的掌握.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 13.6克 | B. | 8.4克 | C. | 3.4 克 | D. | 2.8克 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ① | A1 | B1 | C1 | D1 |
| 电子数 | 10 | 10 | 10 | 18 |
| ② | A2 | B2 | C2 | D2 |
| 电子数 | 10 | 10 | 10 | 18 |
 .
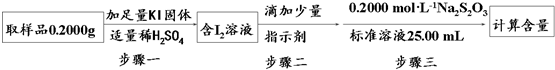
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol | B. | 0.2 mol | C. | 0.3mol | D. | 0.15 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
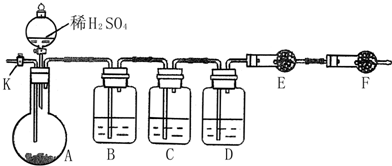
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铝与氨水反应:Al3++3OH-═Al(OH)3↓ | |
| B. | 碳酸钙溶于醋酸:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 过量NaHSO4溶液与少量Ba(OH)2溶液反应:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| D. | NaHCO3溶液中加入氢氧化钠溶液:OH-+HCO3-═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图甲表示lmol H2(g)完全燃烧生成水蒸气吸收241.8kJ热量 | |
| B. | 图甲表示2mol H2(g)所具有的能量比2mol H2O(g)所具有的能量多483.6kJ | |
| C. | 图乙表示常温下稀释HA、HB两种酸的图象,得出结论:HA的酸性大于HB的酸性 | |
| D. | 图乙中起始时HA的物质的量浓度大于HB |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com