
| A. | Fe2O3 与Fe3O4互为同素异形体 | |
| B. | 检验从火星上带回来的红色物质是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液 | |
| C. | 将CO2通入BaCl2溶液中至饱和,有沉淀产生 | |
| D. | 制备Al用电解法,制备Fe、Cu可用还原法 |
分析 A.同素异形体是指同种元素组成的不同单质;
B.氧化铁是难溶于水的氧化物;
C.盐酸的酸性大于碳酸,则二者不反应;
D.由金属活泼性可知,电解氧化铝冶炼Al,还原剂还原Fe、Cu的化合物冶炼金属Fe、Cu.
解答 解:A.同素异形体是指同种元素组成的不同单质,Fe2O3 与Fe3O4是铁的不同氧化物,不是单质,二者不互为同素异形体,故A错误;
B.操作步骤中粉碎后加水氧化铁不能溶解,溶液中无法证明受否含有铁离子,故操作错误,应溶于盐酸再加KSCN检验,故B错误;
C.盐酸的酸性大于碳酸,将CO2通入BaCl2溶液中至饱和,不反应,故C错误;
D.由金属活泼性可知金属冶炼方法,电解氧化铝冶炼Al,还原剂还原Fe、Cu的化合物冶炼金属Fe、Cu,故D正确;
故选D.
点评 本题考查金属及化合物的性质,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | BaCl2+K2SO4═BaSO4↓+2KCl | B. | BaCO3+H2SO4═BaSO4↓+CO2↑+H2O | ||
| C. | Ba(NO3)2+H2SO4═BaSO4↓+2HNO3 | D. | Ba(OH)2+2KHSO4═BaSO4↓+K2SO4+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
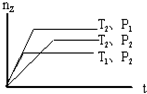 反应 2X(g)+Y(g)?2Z(g),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nZ)与反应时间(t)的关系如图所示.下列判断正确的是( )
反应 2X(g)+Y(g)?2Z(g),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nZ)与反应时间(t)的关系如图所示.下列判断正确的是( )| A. | T1<T2,P1<P2,△H<0 | B. | T1<T2,P1>P2,△H>0 | ||
| C. | T1>T2,P1>P2,△H<0 | D. | T1>T2,P1<P2,△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
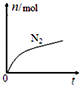
| A. | 该反应的还原剂是Cl- | |
| B. | 消耗1 mol还原剂,转移6 mol电子 | |
| C. | 氧化剂与还原剂的物质的量之比为2:3 | |
| D. | 反应后溶液的酸性明显增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 苯甲酸苯酯是重要的有机合成中间体,工业上用二苯甲酮制备苯甲酸苯酯.
苯甲酸苯酯是重要的有机合成中间体,工业上用二苯甲酮制备苯甲酸苯酯.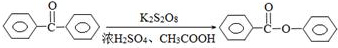
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
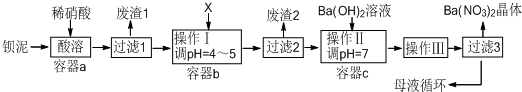
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可以用铜丝或铁丝代替铂丝 | |
| B. | 用固体样品或配成的溶液进行实验,现象相同 | |
| C. | 每次实验前,铂丝要先用硫酸洗涤 | |
| D. | 焰色反应实验所用火焰,无论何种燃料均可 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com