
【题目】现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
科目:高中化学 来源: 题型:
【题目】【化学-有机化学基础】聚合物F的合成路线图如下:
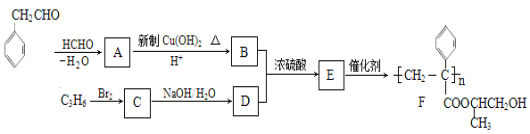
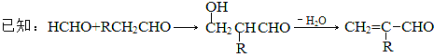
请据此回答:
(1) A中含氧官能团名称是_______,C的系统命名为_________。
(2) 检验B中所含官能团所用的试剂有______;E→F的反应类型是___________。
(3)C生成D的反应化学方程式为_____________________________,如果C与NaOH的醇溶液反应,则生成的有机物的结构简式为___________(同一个碳原子上连两个碳碳双键的除外)。
(4)G物质与![]() 互为同系物,且G物质的相对分子质量比
互为同系物,且G物质的相对分子质量比![]() 大14的,则符合下列条件的G的同分异构体有__________种。
大14的,则符合下列条件的G的同分异构体有__________种。
① 分子中含有苯环,且苯环上有两个取代基 ② 遇氯化铁溶液变紫色 ③ 能与溴水发生加成反应
(5) 参照上述合成路线,设计一条由甲醛、乙醛和甲醇为主要原料制备 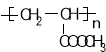 的合成路线 。
的合成路线 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知:FeS2中S为-1价,Cu2S中S为-2价。对于反应l4CuSO4+5FeS2+12H2O =7Cu2S+5FeSO4+12H2SO4,下列说法正确的是( )
A.只有硫酸铜作氧化剂
B.SO42-既不是氧化产物又不是还原产物
C.被氧化的硫与被还原的硫的质量比为3:7
D.1 mol硫酸铜可以氧化5/7 mol的硫原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】树德中学高2016级研宄性学习小组请你参与“研究铁与水反应所得固体物质的成分,性质及再利用”实验探宄,并共同解答下列问题:
探究一 设计如图所示装置进行“铁与水反应”的实验

(1)硬质玻璃管中发生反应的化学方程式为__________________。
(2)反应前A中投放碎瓷片的日的是__________________。
(3)装置E中的现象是__________________。
探究二 设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分。
(4)硬质玻璃管B冷却后,取少许其中的固体物质溶于后,将所得溶液分成两份。
(5)一份滴加儿滴KSCN溶液。若溶液变m红色,推断硬质玻璃管B中固体物质的成分为______________(选填序号,①一定有Fe3O4 ②一定有Fe ③只有Fe3O4④只有Fe,下同);若溶液未变血红色,推断硬质玻璃管B中固体物质的成分为______________。
(6)另—份用胶头滴管加入_______________,若出现______________现象,可以证明溶液中存在Fe2+,其反应的离子方程式是_____________。
探究三 设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。

(7)试剂b的化学式是_________。
(8)计算反应后B装置中铁元素的质量分数为_______________。(保留小数点后—位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素( )
A.在自然界中只以化合态的形式存在
B.单质常用作半导体材料和光导纤维
C.最高价氧化物不与酸反应
D.气态氢化物比甲烷稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,向20mL 0.1mol·L-1的醋酸溶液中不断滴入0.1 mol·L-1的NaOH溶液,溶液的pH变化曲线如图所示.在滴定过程中,关于溶液中离子浓度大小关系的描述,正确的是
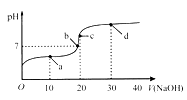
A.a点时:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
B.b点时:c(Na+)=c(CH3COO-)
C.c点时:c(H+)=c(CH3COOH)+c(OH-)
D.d点时:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
①点燃酒精灯进行加热
②在试管中加入2-3ml液体
③用试管夹夹持在试管的中上部
④将试剂瓶的瓶盖盖好,放在原处。
A. ②③④① B. ③②④① C. ②④③① D. ③②①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关“电离平衡”的叙述正确的是( )
A. 电解质在溶液里达到电离平衡时,分子的浓度和离子的浓度相等
B. 电离平衡时,由于分子和离子的浓度不再发生变化,所以说电离平衡是静态平衡
C. 弱电解质达到电离平衡后,各种离子的浓度一定相等
D.电离平衡是相对的、暂时的、外界条件改变时,平衡就会发生移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼泥主要由MgO和SiO2组成,含有少量Fe2O3、FeO、Al2O3等杂质。用硼泥生产氢氧化镁的工艺流程如下图所示:
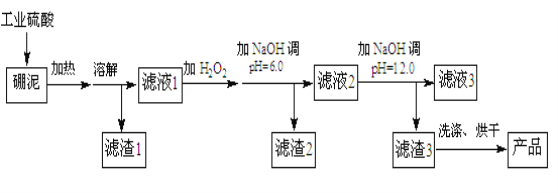
已知某些氢氧化物沉淀的pH如下表所示:
氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
Mg(OH)2 | 9.3 | 10.8 |
Fe(OH)2 | 7.6 | 9.6 |
Al(OH)3 | 4.1 | 5.4 |
Fe(OH)3 | 2.7 | 3.7 |
(1)MgO的电子式为 ,加入H2O2的目的是______________。
(2)滤渣2的主要成分是 ,向滤渣2中继续加入过量的NaOH溶液,发生反应的离子方程式为 。
(3)加入NaOH调节溶液pH=12.0时,发生反应的离子方程式为 。
(4)利用Mg(OH)2与含SO2的烟气反应生成MgSO4,可以使烟气脱硫,该反应的化学方程式为 。
(5)若取a吨硼泥为原料,最后得到b吨Mg(OH)2产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为 (用含有a、b的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com