
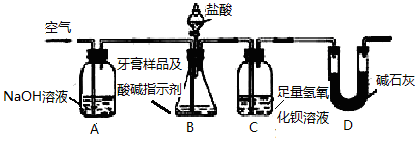
分析 装置先用通过氢氧化钠溶液的空气排净装置内空气,装置B中牙膏样品加入指示剂滴入盐酸全部反应,生成的二氧化碳气体通过装置C中氢氧化钡溶液全部吸收,装置D是防止空气中二氧化碳、水蒸气进入影响测定结果,最后通入空气吧生成的二氧化碳气体全部赶入装置C中完全吸收,
(1)二氧化碳与氢氧化钡反应生成碳酸钡与水;
(2)D是防止空气中二氧化碳和水蒸气进入影响测定结果;
(3)实验通过C装置生成的碳酸钡的质量测定二氧化碳的质量,进而计算牙膏中碳酸钙的质量分数.装置中残留部分二氧化碳,不能被完全吸收,导致测定的碳酸钡的质量偏小;
(4)a、在加入盐酸之前,应排净装置内的CO2气体,防止影响碳酸钡质量的测定;
b、滴加盐酸过快CO2,CO2不能完全被吸收,排出装置C;
c、在AB之间增添盛有浓硫酸的洗气装置,吸收水分,不影响CO2;
d、在BC之间增添盛有饱和碳酸氢钠溶液的洗气装置Ba(OH)2,可以吸收CO2中的HCl,而不影响CO2;
(5)BaCO3质量为3.94g n(BaCO3)=0.0200mol,则n(CaCO3)=0.0200mol,质量为2.00g;
(6)B中的水蒸气、氯化氢气体等进入装置C中.
解答 解:(1)二氧化碳与氢氧化钡反应生成碳酸钡与水,反应方程式为CO2+Ba(OH)2═BaCO3↓+H2O,
故答案为:CO2+Ba(OH)2═BaCO3↓+H2O;
(2)装置D的作用是防止空气中二氧化碳和水蒸气进入影响测定结果,
故答案为:防止空气进入C装置;
(3)装置中残留部分二氧化碳,不能被完全吸收,导致测定的碳酸钡的质量偏小,持续缓缓通入空气的作用为:把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收,
故答案为:把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收;
(4)a、在加入盐酸之前,应排净装置内的CO2气体,防止影响碳酸钡质量的测定,可以提高测定准确度,故a不符合;
b、滴加盐酸过快CO2,CO2来不及被吸收,就排出装置C,滴加盐酸不宜过快,使二氧化碳吸收完全,可以提高测定准确度,故b不符合;
c、在AB之间增添盛有浓硫酸的洗气装置,吸收水分,不影响CO2,不能提高提高测定准确度,故c符合;
d、在BC之间增添盛有饱和碳酸氢钠溶液的洗气装置Ba(OH)2,可以吸收CO2中的HCl,影响CO2,不能提高测定准确度,故d符合.
故答案为:cd;
(5)BaCO3质量为3.94g,则n(BaCO3)=$\frac{3.94g}{197g/mol}$=0.02mol,
则n(CaCO3)=0.02mol,质量为0.02mol×100g/mol=2g,
所以样品中碳酸钙的质量分数为$\frac{2g}{10.0g}$×100%=20%,
故答案为:20%;
(6)B中的水蒸气、氯化氢气体等进入装置C中,导致测定二氧化碳的质量偏大,测定的碳酸钙的质量偏大,碳酸钙的质量分数偏高.
故答案为:B中的水蒸气、氯化氢气体等进入装置C中.
点评 本题考查对实验原理与操作步骤的理解及评价、常用化学用语、化学计算、物质组成的测定等,难度中等,是对所需知识的综合运用,需要学生具有扎实的基础知识与分析问题、解决问题的能力,理解实验原理是解答的关键.


科目:高中化学 来源: 题型:选择题
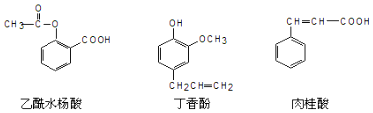
| A. | ②与③ | B. | ③与④ | C. | ①与④ | D. | ①与② |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
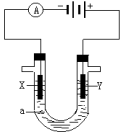 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲=乙>丙 | B. | 丙>甲=乙 | C. | 甲>乙>丙 | D. | 甲>丙>乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径 A>B>D>C | B. | 原子序数 D>C>B>A | ||
| C. | 离子半径 C>D>B>A | D. | 单质的还原性 A>B>D>C |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com