
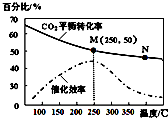
| A£® | Éś³ÉŅŅĻ©µÄĖŁĀŹ£ŗv£ØM£©ÓŠæÉÄÜŠ”ÓŚv£ØN£© | |
| B£® | Ę½ŗā³£Źż£ŗKM£¾KN | |
| C£® | µ±ĪĀ¶ČøßÓŚ250”ę£¬ÉżøßĪĀ¶Č£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬“Ó¶ųŹ¹“߻ƼĮµÄ“߻Ɗ§ĀŹ½µµĶ | |
| D£® | ČōĶ¶ĮĻ±Čn£ØH2£©£ŗn£ØCO2£©=3£ŗ1£¬ŌņĶ¼ÖŠMµćŹ±£¬ŅŅĻ©µÄĢå»ż·ÖŹżĪŖ7.7% |
·ÖĪö A”¢ĪĀ¶ČÉżøß»Æѧ·“Ó¦ĖŁĀŹ¼Óæģ£¬“߻ƼĮµÄ“߻Ɗ§ĀŹ½µµĶ£»
B”¢ÉżøßĪĀ¶Č¶žŃõ»ÆĢ¼µÄĘ½ŗā×Ŗ»ÆĀŹ¼õµĶ£¬ŌņÉżĪĀĘ½ŗāÄęĻņŅĘ¶Æ£»
C”¢øł¾ŻĶ¼Ļ󣬵±ĪĀ¶ČøßÓŚ250”ę£¬ÉżøßĪĀ¶Č¶žŃõ»ÆĢ¼µÄĘ½ŗā×Ŗ»ÆĀŹ¼õµĶ£¬ŌņĘ½ŗāÄęĻņŅĘ¶Æ£»
D”¢ÉčæŖŹ¼Ķ¶ĮĻn£ØH2£©ĪŖ3mol£¬Ōņn£ØCO2£©ĪŖ1mol£¬ĖłŅŌµ±ŌŚMµćĘ½ŗāŹ±¶žŃõ»ÆĢ¼µÄ×Ŗ»ÆĀŹĪŖ50%£¬¾Ż“ĖĮŠČż¶ĪŹ½¼ĘĖć£®
½ā“š ½ā£ŗA”¢»Æѧ·“Ó¦ĖŁĀŹĖęĪĀ¶ČµÄÉżø߶ų¼Óæģ£¬“߻ƼĮµÄ“߻Ɗ§ĀŹ½µµĶ£¬ĖłŅŌv£ØM£©ÓŠæÉÄÜŠ”ÓŚv£ØN£©£¬¹ŹAÕżČ·£»
B”¢ÉżøßĪĀ¶Č¶žŃõ»ÆĢ¼µÄĘ½ŗā×Ŗ»ÆĀŹ¼õµĶ£¬ŌņÉżĪĀĘ½ŗāÄęĻņŅĘ¶Æ£¬ĖłŅŌM»ÆŃ§Ę½ŗā³£Źż“óÓŚN£¬¹ŹBÕżČ·£»
C”¢øł¾ŻĶ¼Ļ󣬵±ĪĀ¶ČøßÓŚ250”ę£¬ÉżøßĪĀ¶Č¶žŃõ»ÆĢ¼µÄĘ½ŗā×Ŗ»ÆĀŹ¼õµĶ£¬ŌņĘ½ŗāÄęĻņŅĘ¶Æ£¬µ«“߻ƼĮÖ»Ó°Ļģ·“Ó¦ĖŁĀŹ£¬²»Ó°ĻģĘ½ŗāŅʶÆŗĶ×Ŗ»ÆĀŹ£¬ĖłŅŌÓė“߻ƼĮµÄ“߻Ɗ§ĀŹ½µµĶĪŽŅņ¹ū¹ŲĻµ£¬¹ŹC“ķĪó£»
D”¢ÉčæŖŹ¼Ķ¶ĮĻn£ØH2£©ĪŖ3mol£¬Ōņn£ØCO2£©ĪŖ1mol£¬ĖłŅŌµ±ŌŚMµćĘ½ŗāŹ±¶žŃõ»ÆĢ¼µÄ×Ŗ»ÆĀŹĪŖ50%
ĖłŅŌÓŠ6H2£Øg£©+2CO2£Øg£©$\stackrel{“߻ƼĮ}{?}$CH2=CH2£Øg£©+4H2O£Øg£©
æŖŹ¼ 3 1 0 0
×Ŗ»Æ 1.5 0.5 0.25 1
Ę½ŗā 1.5 0.5 0.25 1
ĖłŅŌŅŅĻ©µÄĢå»ż·ÖŹżĪŖ$\frac{0.25}{1.5+0.5+0.25+1}$”Į100%=7.7%£¬¹ŹDÕżČ·£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĮĖĶ¼Ļó·ÖĪö»Æѧ·“Ó¦ĖŁĀŹµÄÓ°ĻģŅņĖŲ”¢Ę½ŗā¼ĘĖć”¢Ę½ŗāŅĘ¶ÆµČ£¬ĢāÄæÄŃ¶Č²»“ó£®


 53ĖęĢĆ²āĻµĮŠ“š°ø
53ĖęĢĆ²āĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÅØĮņĖį | B£® | ¼īŹÆ»Ņ | C£® | ¹żŃõ»ÆÄĘ | D£® | »īŠŌĢæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
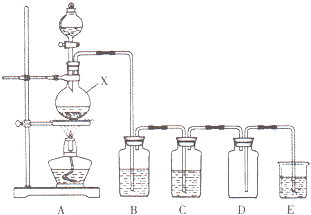 ŹµŃéŹŅÖŠ³£ÓƶžŃõ»ÆĆĢÓėÅØŃĪĖį¹²ČČÖĘČ”ĀČĘų£®Ä³»ÆѧŠĖȤŠ”×éĪŖÖĘČ”½ĻĪŖ“æ¾»”¢øÉŌļµÄĀČĘų£¬Éč¼ĘĮĖČēĻĀŹµŃé×°ÖĆ£®
ŹµŃéŹŅÖŠ³£ÓƶžŃõ»ÆĆĢÓėÅØŃĪĖį¹²ČČÖĘČ”ĀČĘų£®Ä³»ÆѧŠĖȤŠ”×éĪŖÖĘČ”½ĻĪŖ“æ¾»”¢øÉŌļµÄĀČĘų£¬Éč¼ĘĮĖČēĻĀŹµŃé×°ÖĆ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | 0”«t2Ź±£¬vÕżŹ¼ÖÕ“óÓŚvÄę | |
| B£® | ¢ń”¢¢ņĮ½¹ż³Ģ“ļµ½Ę½ŗāŹ±£¬AµÄĢå»ż·ÖŹż¢ń£¾¢ņ | |
| C£® | ¢ń”¢¢ņĮ½¹ż³Ģ“ļµ½Ę½ŗāŹ±£¬Ę½ŗā³£Źż¢ń£¼¢ņ | |
| D£® | t2Ź±æĢøıäµÄĢõ¼žæÉŅŌŹĒĻņĆܱÕČŻĘ÷ÖŠ¼ÓC |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
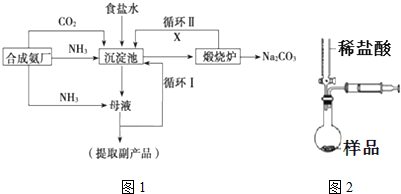
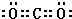 £¬³Įµķ³ŲÖŠ·¢ÉśµÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ£ŗCO2+NH3+NaCl+H2OØTNaHCO3”ż+NH4Cl£®
£¬³Įµķ³ŲÖŠ·¢ÉśµÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ£ŗCO2+NH3+NaCl+H2OØTNaHCO3”ż+NH4Cl£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŠņŗÅ | ²Ł×÷¼°ĻÖĻó | ½įĀŪ |
| A | Ļņ2mL1mol/LNaOHČÜŅŗÖŠĻČ¼ÓČė3µĪ1mol/LMgCl2ČÜŅŗ£¬ŌŁ¼ÓČė3µĪ1mol/LFeCl3 | Mg£ØOH£©2×Ŗ»ÆĪŖFe£ØOH£©3 |
| B | ³£ĪĀĻĀ£¬²āµĆ±„ŗĶNa2CO3ČÜŅŗµÄpH“óÓŚ±„ŗĶNaHCO3ČÜŅŗ | ³£ĪĀĻĀĖ®½ā³Ģ¶Č£ŗCO32-£¾HCO3- |
| C | Ļņ25mLĄäĖ®ŗĶ·ŠĖ®ÖŠ·Ö±šµĪČė5µĪFeCl3±„ŗĶČÜŅŗ£¬Ē°ÕßĪŖ»ĘÉ«£¬ŗóÕßĪŖŗģŗÖÉ« | ĪĀ¶ČÉżøߣ¬Fe3+µÄĖ®½ā³Ģ¶ČŌö“ó |
| D | äåŅŅĶéÓėNaOHŅŅ“¼ČÜŅŗ¹²ČČ²śÉśµÄĘųĢåĶØČėKMnO4ĖįŠŌČÜŅŗÖŠ£¬ČÜŅŗĶŹÉ« | ²śÉśµÄĘųĢåĪŖŅŅĻ© |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ćŗ”¢ŹÆÓĶŗĶĢģČ»Ęų¶¼ŹĒÖŲŅŖµÄ»ÆŹÆČ¼ĮĻ | |
| B£® | ²ĻĖ攢ĖÜĮĻŗĶĻš½ŗ¾łŹōÓŚŗĻ³Éøß·Ö×Ó²ÄĮĻ | |
| C£® | µķ·Ū”¢ĀóŃæĢĒŗĶµ°°×ÖŹ¾łÄÜ·¢ÉśĖ®½ā·“Ó¦ | |
| D£® | ĢĒĄą”¢ÓĶÖ¬ŗĶµ°°×ÖŹ¶¼ŗ¬ÓŠC”¢H”¢OČżÖÖŌŖĖŲ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com