
| A. | KCl(NH4Cl)用加热法分离 | B. | CO2(SO2)通过饱和的碳酸钠溶液洗气 | ||
| C. | NO(NO2)通过水洗气 | D. | FeCl3溶液(FeCl2)通入氯气 |
分析 A.NH4Cl受热易分解;
B.二氧化碳能与碳酸钠反应生成碳酸氢钠;
C.NO2可与水反应生成NO;
D.亚铁离子和氯气反应能生成铁离子.
解答 解:A.NH4Cl受热易分解,氯化钾受热稳定,可分离,故A正确;
B.二氧化碳能与碳酸钠反应生成碳酸氢钠,将原物质除掉,故B错误;
C.NO2可与水反应生成NO,且NO不溶于水,故C正确;
D.因为亚铁离子和氯气反应能生成铁离子,化学方程式为2FeCl2+Cl2═2FeCl3,而且不引入新的杂质,故可用氯气除去FeCl3溶液中少量的FeCl2,故D正确.
故选B.
点评 本题考查混合物的分离提纯,为高频考点,把握物质的性质、发生的反应、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的综合应用,题目难度不大.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:解答题
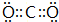 ;元素Z的离子结构示意图为
;元素Z的离子结构示意图为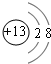 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
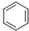 +CH3CH2CH2Cl$\stackrel{催化剂}{→}$
+CH3CH2CH2Cl$\stackrel{催化剂}{→}$ 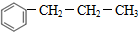 +HCl
+HCl
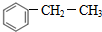 ,F的结构简式为
,F的结构简式为 ,
, .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤ | B. | ②③④ | C. | ①④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素(或元 素代码) | 铍 | A | B | C | D | E | F |
| 原子半径 (10-10m) | 0.89 | 1.60 | 1.43 | 0.75 | 0.74 | 1.02 | 0.99 |
| 最高价态 | +2 | +2 | +3 | +5 | - | +6 | +7 |
| 最低价态 | - | - | - | -3 | -2 | -2 | -1 |
 .
. .它与C元素最高价氧化物水化物反应的生成物是属于离子(离子或共价)化合物,其中含有的化学键类型有离子键、共价键.
.它与C元素最高价氧化物水化物反应的生成物是属于离子(离子或共价)化合物,其中含有的化学键类型有离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | X | Y | Z | M |
| A | H2S | S | SO3 | O2 |
| B | Mg | C | CO | CO2 |
| C | NaOH | Na2CO3 | NaHCO3 | CO2 |
| D | NH3 | NO | NO2 | O2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向滴加有KSCN的FeCl2溶液,不断滴加氯水 | 溶液颜色先变红后褪色 | Fe2+先是被氧化为Fe3+,后来又被还原为Fe2+ |
| B | 向浓盐酸中加入少量碳酸钠溶液,将产生的气体通入苯酚钠溶液 | 苯酚钠溶液中出现白色浑浊 | 实验有缺陷,不能证明酸性:盐酸>碳酸>苯酚 |
| C | 在酸性KMnO4溶液中通入SO2 | 溶液褪色 | SO2具有漂白性 |
| D | 用标准浓度的烧碱溶液滴定未知浓度的盐酸,酚酞做指示剂 | 锥形瓶内溶液颜色由无色变为浅红色立即停止滴定 | 酸碱恰好中和 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com