
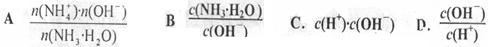
 4)将________。
4)将________。 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源:不详 题型:单选题
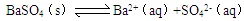 的下列说法正确的是( )
的下列说法正确的是( )| A.溶液的温度升高,BaSO4的溶度积常数不变 |
| B.在Na2SO4溶液中,BaSO4的溶解度不变 |
| C.在BaCl2溶液中,BaSO4的溶度积常数变小 |
| D.精制NaCl时,在溶液中加入稍过量的BaCl2溶液是为了更好地除去SO42-等离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

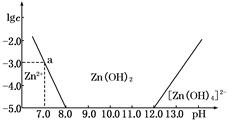
 Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O Cr3+(aq)+3OH—(aq)
Cr3+(aq)+3OH—(aq)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
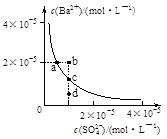
| A.加入Na2SO4可以使溶液由a点变到b点 |
| B.通过蒸发可以使溶液由d点变到c点 |
| C.d点无BaSO4沉淀生成 |
| D.a点对应的BaSO4的Ksp大于c点对应的Ksp |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH增大 |
B.AgCl悬浊液中存在平衡:AgCl(s) 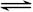 Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小 Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小 |
| C.为减小洗涤过程中固体的损失,最好选用稀H2SO4代替H2O来洗涤BaSO4沉淀 |
| D.硬水中含有较多的Ca2+、Mg2+、HCO3-、SO42-,加热煮沸可以完全除去其中的 Ca2+、Mg2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| c(HCl) | | | | | | | |
| (mol/L) | 0.50 | 1.00 | 2.04 | 2.90 | 4.02 | 5.16 | 5.78 |
| 103c(PbCl2) | | | | | | | |
| (mol/L) | 5.10 | 4.91 | 5.21 | 5.90 | 7.48 | 10.81 | 14.01 |
| A.随着盐酸浓度的增大,PbCl2固体的溶解度先变小后又变大 |
| B.PbCl2固体在0.50 mol/L盐酸中的溶解度小于在纯水中的溶解度 |
| C.PbCl2能与浓盐酸反应生成一种难电离的阴离子(络合离子) |
| D.PbCl2固体可溶于饱和食盐水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.AgCl沉淀生成和沉淀溶解不断进行,但速率相等 |
| B.在此饱和溶液中加水,KSP(AgCl)增大 |
| C.在此饱和溶液中加浓的Na2S溶液,生成黑色沉淀 |
| D.向AgCl饱和溶液中加入NaCl固体,c(Ag+)不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 .盐碱地(含较多NaCl、Na2CO3)不利于作物生成,通过施加适量石膏(CaSO4)可以降低土壤的碱性。
.盐碱地(含较多NaCl、Na2CO3)不利于作物生成,通过施加适量石膏(CaSO4)可以降低土壤的碱性。 加入石膏降低土壤碱性的反应原理 ;
加入石膏降低土壤碱性的反应原理 ; 请分析水垢中的CaSO4转化为CaCO3的原理 ;
请分析水垢中的CaSO4转化为CaCO3的原理 ;查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
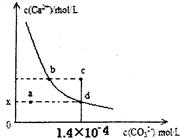
| A.x的数值为2×10-5 |
| B.c点时有CaCO3生成 |
| C.加入蒸馏水可使溶液由d点变成 a点 |
| D.b点与d点对应的溶度积相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com