
【题目】某化学兴趣小组设计如下实验方案。将浓硫酸与铜片反应制备SO2并进行相关实验探究,实验装置如下图所示:
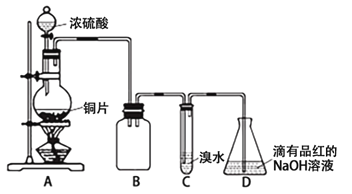
请回答下列问题:
(1)装置B的作用是 。
(2)设计装置C的目的是验证SO2的 性,装置C中发生反应的离子方程式是 。装置D中NaOH全部转化为NaHSO3的标志是 。
(3)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能的情况:
I.HSO3-与ClO-恰好反应
Ⅱ.NaClO不足
Ⅲ.NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请完成下表:(已知酸性:H2SO3>H2CO3>HClO)
(4)请设计简单实验证明:室温下HSO3-的电离平衡常数Ka与水解平衡常数Kb的相对大小: 。
【答案】(14分)
(1)防倒吸(或安全瓶)(1分)
(2)还原(1分);SO2 + Br2 + 2H2O === 4H+ + SO42- + 2Br- (2分)
溶液由红色变为无色 (2分)
(3)②溶液变为蓝色 (2分) ③溴水褪色(2分)
④Ⅰ或 Ⅲ(2分,仅填其中1个得1分)
[提示:发生的反应为 HSO3-+ClO-=== H++SO42-+Cl-]
(4)常温下,用pH试纸(或pH计)测定NaHSO3溶液的pH,若pH<7,则Ka>Kb ;若 pH>7,则Ka<Kb (2分)(其它合理答案也可给分)
【解析】
试题分析:由图可知,A中发生Cu与浓硫酸的反应生成二氧化硫,B作安全瓶,可防止倒吸,C中发生SO2+Br2+2H2O=H2SO4+2HBr,D中NaOH溶液吸收尾气,
(1)装置B的作用是防倒吸(或安全瓶),故答案为:防倒吸(或安全瓶);
(2)C中发生的反应中S元素的化合价升高,则设计装置C的目的是验证SO2的还原性,装置C中发生反应的离子方程式是SO2+Br2+2H2O=4H++SO42-+2Br-.装置D中NaOH全部转化为NaHSO3时碱性降低,装置D中NaOH全部转化为NaHSO3的标志是溶液由红色变为无色,
故答案为:还原;SO2+Br2+2H2O=4H++SO42-+2Br-;溶液由红色变为无色;
(3)②NaClO可氧化KI,则观察到溶液变为蓝色;
③溴水可氧化HSO3-,则观察到溴水褪色,
④HSO3-与高锰酸钾可发生氧化还原反应,由溶液为紫色可知,不存在HSO3-,则I或Ⅲ成立,
故答案为:
序号 | 实 验操作 | 现 象 | 结 论 |
① | 加几小块CaCO3固体 | 有气泡产生 | I或Ⅱ |
② | 滴加少量淀粉KI溶液,振荡 | 溶液变为蓝色 | Ⅲ |
③ | 滴加少量溴水,振荡 | 溴水褪色 | Ⅱ |
④ | 滴加少量酸性KMn04溶液、振荡 | 溶液为紫色 | I或Ⅲ |
(4)电离显酸性,水解显碱性,则测定pH即可,则设计实验为常温下,用pH试纸(或pH计)测定NaHS03溶液的pH,若pH<7,则Ka>Kb,若pH>7,则Ka<Kb,
故答案为:常温下,用pH试纸(或pH计)测定NaHS03溶液的pH,若pH<7,则Ka>Kb,若pH>7,则Ka<Kb。


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会等密切相关,下列说法正确的是
A. 绿色化学的核心是应用化学原理对环境污染进行治理
B. 用CO2合成可降解的聚碳酸酯塑料,能减少白色污染及其危害
C. 推广使用煤的液化技术,从根本上减少二氧化碳等温室气体的排放
D. 明矾常用于水体杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计实验,测定Na2CO3与NaHCO3混合物中Na2CO3的质量分数。
甲方案:
实验步骤为:①称量空坩埚的质量为A g;②称量装有试样的坩埚质量为B g;③加热;④冷却;⑤称量坩埚和残余物的质量为C g;⑥重复③至⑤操作,直至恒重,质量为D g。
(1)坩埚中发生反应的化学方程式 。
(2)计算Na2CO3质量分数必须用到的测定数据为 。
乙方案:
在天平上准确称取 0.3000g样品,放入锥形瓶中,加入适量水溶解,滴入2滴酚酞试液,用0.1000mol·L-1的标准盐酸滴定至溶液由粉红色刚好变为无色,达到滴定终点时产物为NaHCO3,即HCl+Na2CO3 == NaHCO3+NaCl。重复上述操作两次。
(3)配制上述盐酸标准溶液100ml,若用2.0mol/LHCl进行配制,需用量筒量取该HCl溶液 ml;定容时俯视刻度线,将导致配制的溶液浓度 。(填“偏高”、“偏低”或“没有影响”)
(4)根据下表数据,样品中w(Na2CO3)= 。(用百分数表示,保留一位小数)
滴定次数 | 样品的质量/g | 稀盐酸的体积/mL | |
滴定前刻度/mL | 滴定后刻度/mL | ||
1 | 0.3000 | 1.02 | 21.03 |
2 | 0.3000 | 2.00 | 21.99 |
3 | 0.3000 | 0.20 | 20.20 |
丙方案:
称取m g样品,选用下图部分装置测定样品与硫酸反应生成的气体体积。
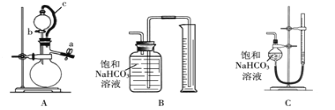
(5)某同学按以下方法检查装置A的气密性:在分液漏斗中加入适量水,如图连接好装置,关闭止水夹a,用止水夹夹住橡皮管c,打开活塞b。若分液漏斗中的水无法持续滴下,试判断装置A是否漏气? (填“漏气”、“不漏气”或“无法确定”)。实验时,装置A中c的作用 , 。
(6)为了提高测定的准确性,应选用装置A和 (填写字母标号)进行实验。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲是一种含有结晶水的盐,由A、B、C、D、E五种元素组成,其中四种是短周期元素。甲溶于水后可电离出两种阳离子和一种阴离子,其中A、B两元素可形成10电子的阳离子。A元素原子核内质子数比E的少1,D、E处于同主族。
用甲进行如下实验:
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中滴入KSCN溶液,无现象,再滴入过氧化氢的酸性溶液,呈红色;
③取少量甲溶液于试管中,向其中加入稀盐酸后,再加入BaCl2溶液,出现白色沉淀;
④取少量甲溶液于试管中加入适量NaOH溶液,加热;
回答下列问题:
(1)实验③可证明溶液中含有 。
(2)用离子方程式表示实验②中现象的原因: , 。
(3)实验④中出现的现象是 。
(4)经测定甲晶体的摩尔质量为392 g/mol,其中阳离子与阴离子物质的量之比为3:2,则甲晶体的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体NaOH因吸收了空气中的CO2而含有杂质,现在要将该固体NaOH配制成较纯的溶液,则其主要的实验操作过程应是( )
A.溶解、加适量BaCl2溶液、过滤
B.溶解、加适量CaCl2溶液、过滤
C.溶解、加适量Ca(OH)2溶液、过滤
D.溶解、加适量盐酸、加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机玻璃( )因具有良好的性能而广泛应用于生产生活中。下图所示流程可用于合成有机玻璃,请回答下列问题:
)因具有良好的性能而广泛应用于生产生活中。下图所示流程可用于合成有机玻璃,请回答下列问题:

(1)A的名称为_______________;
(2)B→C的反应条件为_______________;D→E的反应类型为_______________;
(3)两个D分子间脱水生成六元环酯,该酯的结构简式为______________;
(4)写出下列化学方程式:
G→H:_______________________________;
F→有机玻璃:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项操作错误的是 ( )
A.用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液
B.进行分液时,分液漏斗中的下层液体从下端流出,上层液体则从上口倒出
C.萃取、分液前需对分液漏斗检漏
D.为保证分液漏斗内的液体顺利流出,需将上面的塞子拿下(或使塞上的凹槽对准漏斗上的小孔)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com