
| 2.4g |
| 160g/mol |
| 0.03mol×56g/mol |
| 3.31g |
| 0.637g |
| 16g/mol |


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、称量、溶解、蒸发结晶、过滤、洗涤、干燥 |
| B、称量、溶解、蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
| C、溶解、蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
| D、溶解、蒸发结晶、过滤、洗涤、干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
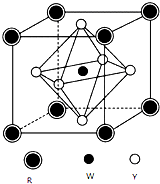 前四周期元素X、Y、Z、W、R的原子序数依次增大,已知:X原子的2p轨道为半充满状态;Y原子的L层有2个未成对电子;Z与Y位于同主族;W的+2价简单离子核外电子层排布与Ar原子相同;R原子的d轨道上有3个空轨道.请回答下列问题:
前四周期元素X、Y、Z、W、R的原子序数依次增大,已知:X原子的2p轨道为半充满状态;Y原子的L层有2个未成对电子;Z与Y位于同主族;W的+2价简单离子核外电子层排布与Ar原子相同;R原子的d轨道上有3个空轨道.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
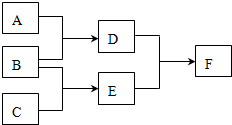 现有 D、E、F六种物质,其中A、B、C是由短周期元素组成的常见单质,D分子含有10个电子,F是一种不含金属元素的盐.一定条件下转化关系如下:请回答:
现有 D、E、F六种物质,其中A、B、C是由短周期元素组成的常见单质,D分子含有10个电子,F是一种不含金属元素的盐.一定条件下转化关系如下:请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、全正确 | B、①②③④⑥ |
| C、②③④⑤ | D、③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Q=Q1+Q2+Q3 | ||
| B、Q=Q1-Q2-Q3 | ||
C、Q=
| ||
D、Q=
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com