
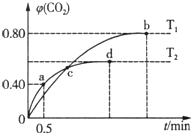
 利用I2O5消除CO污染的反应为:5CO(g)+I2O5(s)?5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4mol CO,测得CO2的体积分数随时间t变化曲线如图.下列说法不正确的是( )
利用I2O5消除CO污染的反应为:5CO(g)+I2O5(s)?5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4mol CO,测得CO2的体积分数随时间t变化曲线如图.下列说法不正确的是( )| A. | T2时,0~0.5 min内的反应速率v(CO)=1.6mol/(L•min) | |
| B. | 两种温度下,c点时体系中混合气体的压强相等 | |
| C. | d点时,增大体系压强,CO的转化率不变 | |
| D. | b点和d点时化学平衡常数的大小关系:Kb>Kd |
分析 A.根据三段式计算出参加反应的CO的物质的量,再根据v(CO)=$\frac{△c}{△t}$进行计算;
B.c点为交点,各气体物质的量分别相等,但温度不同;
C.反应前后气体体积不变,压强变化对平衡无影响;
D.b点比d点时生成物CO2体积分数大,说明反应进行的程度大.
解答 解:A.a点时:5CO(g)+I2O5(s)?5CO2(g)+I2(s)
起始量/mol 4 0
转化量/mol x x
a点量/mol 4-x x
a点时CO2的体积分数φ(CO2)=$\frac{x}{4}$=0.40,解得x=1.6mol,
T2时,0~0.5 min内的反应速率v(CO)=$\frac{\frac{1.6mol}{2L}}{0.5min}$=1.6mol•L-1•min-1,故A正确;
B.c点为交点,气体物质的量分别相等,所以两种温度下,体系中混合气体的压强不等,故B错误;
C.反应前后气体体积不变,压强变化对平衡无影响,CO的转化率不变,故C正确;
D.b点比d点时生成物CO2体积分数大,说明反应进行的程度大,则化学平衡常数:Kb>Kd,故D正确;
故选B.
点评 本题考查化学反应速率的相关计算、化学平衡移动原理及化学平衡常数的大小判断等知识,难度中等.读懂图象是解题的关键.


科目:高中化学 来源: 题型:选择题
| A. | Fe | B. | Si | C. | Cu | D. | Na |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
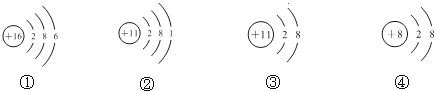
| A. | 它们表示三种元素 | |
| B. | ②③的化学性质相同 | |
| C. | ②表示的元素是金属元素 | |
| D. | ①表示的是原子,而④表示的是阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知Ra是第七周期、IIA族的元素,故Ra(OH)2的碱性比Mg(OH)2的碱性强 | |
| B. | 已知As是第四周期、VA族的元素,故AsH3 的稳定性比NH3的稳定性强 | |
| C. | 已知Cs原子半径比Na的原子半径大,故Cs与水反应比Na与比反应更剧烈 | |
| D. | 已知Cl与Al处于同一周期,且Cl的核电荷数比Al的核电荷数大,故Cl的原子半径比Al的原子半径小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol O2与Na完全反应,转移电子数一定为4NA | |
| B. | 常温常压下,1.7克NH3中含有共价键的数目为NA | |
| C. | 142g Na2SO4和Na2HPO4混合物中含有的阴、阳离子总数是3 NA | |
| D. | 标准状况下,11.2 L SO3所含的分子数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 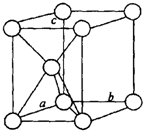 | (1)镁原子在二维空间的配位数为6 |
| (2)位于晶胞中部的鎂原子与离它最近两平面相切(填“相离”或“相切”或”相交”) | |
| (3)请用含R1、NA的数学式子表达金属镁的密度:$\frac{3\sqrt{2}}{{{R}_{1}}^{3}{N}_{A}}$g/cm3(根号带在分子上) | |
 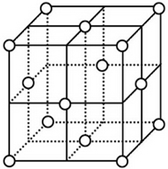 | (4)铜原子在三维空间的配位数为12 |
| (5)晶胞中面心上的六个铜原子构成的空间几何体名称为正八面体 | |
| (6)请用含R2、NA的数学式子表达金属铜的密度:$\frac{8\sqrt{2}}{{N}_{A}{{•R}_{2}}^{3}}$g/cm3(根号带在分子上) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
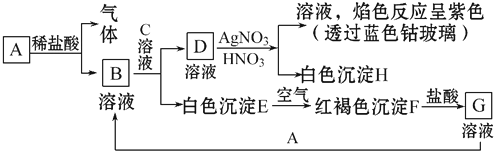
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com