
【题目】电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42﹣ ![]() 2PbSO4+2H2O则下列说法正确的是( )
2PbSO4+2H2O则下列说法正确的是( ) 
A.放电时:电子流动方向由A经导线流向B
B.放电时:正极反应是Pb﹣2e﹣+SO42﹣ ![]() PbSO4
PbSO4
C.充电时:铅蓄电池的负极应与充电器电源的正极相连
D.充电时:阳极反应是PbSO4﹣2e﹣+2H2O=PbO2+SO42﹣+4H+
【答案】D
【解析】解:A.放电时,Pb极即B极为电池负极,PbO2极即A极为正极,电子流动方向由负极经导线流向正极,即由B经导线流向A,故A错误;B、由铅蓄电池的总反应PbO2+2H2SO4+Pb═2PbSO4+2H2O可知,放电时,Pb被氧化,应为电池负极反应,电极反应式为Pb﹣2e﹣+SO42﹣=PbSO4 , 正极上PbO2得电子被还原,电极反应式为PbO2+SO42﹣+2e﹣+4H+═PbSO4+2H2O,故B错误;
C、在充电时,铅蓄电池的负极的逆反应是还原反应,应与充电器电源的负极相连,故C错误;
D、在充电时,阳极上发生氧化反应,和放电时的正极反应互为逆反应,即PbSO4﹣2e﹣+2H2O=PbO2+SO42﹣+4H+ , 故D正确.
故选D.
由铅蓄电池的总反应PbO2+2H2SO4+Pb═2PbSO4+2H2O可知,放电时,Pb被氧化,应为电池负极反应,电极反应式为Pb﹣2e﹣+SO42﹣=PbSO4 , 正极上PbO2得电子被还原,电极反应式为PbO2+SO42﹣+2e﹣+4H+═PbSO4+2H2O,在充电时,阳极上发生氧化反应,电极反应式和放电时的正极反应互为逆反应,阴极上发生还原反应,电极反应式和放电时的负极反应互为逆反应.


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:
【题目】根据要求,回答下列问题:
(1)写出离子反应方程式“Ba2+ + SO42- = BaSO4↓”对应的化学反应方程式____________;
(2)氧化还原反应“2Na + O2 ![]() Na2O2”,氧化产物是_______;氧化剂是_____。
Na2O2”,氧化产物是_______;氧化剂是_____。
(3)维生素C 又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C 具有___。(填氧化性或还原性)
(4)某混合物中可能含有可溶性硫酸盐、碳酸盐及硝酸盐。为了检验其中是否含有硫酸盐,某同学取少量混合物溶于水后,向其中加入_________溶液,再加入______溶液发现有白色沉淀生成,并由此得出该混合物中含有硫酸盐的结论。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某物质中加入浓的氢氧化钠溶液并加热,能产生使润湿的红色石蕊试纸变蓝的气体,该物质可能是
A. MgCl2B. FeCl3C. NaClD. NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:(X代表卤素原子,R代表烃基) ![]()
利用上述信息,按以下步骤从 ![]() 合成
合成 ![]() .(部分试剂和反应条件已略去)
.(部分试剂和反应条件已略去)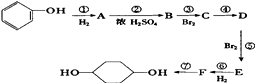
请回答下列问题:
(1)分别写出B,D的结构简式:B、D .
(2)反应①~⑦中属于消去反应的是 . (填数字代号)
(3)如果不考虑⑥、⑦反应,对于反应⑤,得到的E可能的结构简式为: .
(4)试写出C→D反应的化学方程式(有机物写结构简式,并注明反应条件): .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铋(Bi)在医药方面有重要应用.下列关于 ![]() Bi和
Bi和 ![]() Bi的说法正确的是( )
Bi的说法正确的是( )
A.![]() Bi和
Bi和 ![]() Bi都含有83个中子
Bi都含有83个中子
B.![]() Bi和
Bi和 ![]() Bi互为同位素
Bi互为同位素
C.![]() Bi和
Bi和 ![]() Bi的核外电子数不同
Bi的核外电子数不同
D.![]() Bi和
Bi和 ![]() Bi分别含有126和127个质子
Bi分别含有126和127个质子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g)C(g)+D(g)过程中的能量变化如图所示,由此可判断( ) 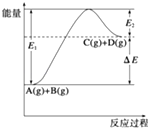
A.1mol A与1mol B充分反应后,能量变化为△E
B.加入催化剂后,反应加快,△E减小
C.反应物的总键能小于生成物的总键能
D.反应达到平衡时,升高温度,A的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g)N2(g)+CO2(g)+2H2O(g)△H=a kJ/mol 在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得n(CH4)随时间变化数据如下表:下列说法不正确的是( )
温度 | 时间/min | 0 | 10 | 20 | 40 | 50 |
T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4) | 0.50 | 0.30 | 0.18 | … | 0.15 |
A.10 min内,T1时CH4的化学反应速率比T2时小
B.温度:T1<T2
C.a<0
D.平衡常数:K(T1)<K(T2)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com