
T��W��X��Y��Z��Ԫ�����ڱ�ǰ�������еij���Ԫ�أ�ԭ�������������������Ϣ���±���
Ԫ�� | �����Ϣ |
T | TԪ�ؿ��γ���Ȼ��Ӳ�����ĵ��� |
W | W��Tͬ���ڣ�����������δ�ɶԵ��� |
X | Xԭ�ӵĵ�һ�����������ĵ����ֱܷ��ǣ�I1=578kJ/mol��I2=1817kJ/mol�� I3=2745kJ/molkJ/mol��I4=11575kJ/mol |
Y | ���³�ѹ�£�Y�����ǹ��壬�����������γ��������Ҫ���� |
Z | Z��һ��ͬλ�ص�������Ϊ63��������Ϊ34 |
��1��Y�����ڱ��е�λ�� ��Y������WԪ�صĵ�һ�������ɴ�С˳��Ϊ ����Ԫ�ط������𣩡�
��2��TY2��һ�ֳ��õ��ܼ����� ����Է��ӻ�Ǽ��Է��ӣ��������д��������Ҽ���
��3��д��X��NaOH��Һ��Ӧ�����ӷ���ʽ �����ߵ��Ⱦ�Ե��������XW�ھ�Ե������Ӧ�ù㷺����������ʯ���ƣ����� ���壮W������⻯������Һ���������� ��
��4��Z�Ļ�̬ԭ�Ӻ�������Ų�ʽΪ ��Ԫ��Z������������е������Լ�������Ӧ�����ɳ����Z��HCl��O2��ZCl��HO2��HO2 �������ᣩ������һ���������Ҳ��һ�����ɻ������м��ߵĻ��ԡ�����˵�����ʾ�������
A����������O2 B��HO2�ڼ��в����ȶ�����
C������������HO2 D��1 molZ�μӷ�Ӧ��1 mol���ӷ���ת��
��5����֪Z�ľ����ṹ����ͼ��ʾ����֪Z���ܶ�Ϊ9��00 g��cm��3�����߳�Ϊ ��ZYO4�������Һ������YO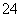 �Ŀռ乹���� ������Yԭ�ӵ��ӻ���������� ��
�Ŀռ乹���� ������Yԭ�ӵ��ӻ���������� ��

���𰸡���1���� ��1�֣���A��1�֣�NOS��1�֣� ��2���Ǽ��Է��ӣ�1�֣� 2��1�֣�
��3��2Al+ 2OH- + 2H2O = 2AlO2- + 3H2����2�֣�ԭ�Ӿ��壨1�֣����Ӽ��γ������1�֣�
��4��[Ar]3d104s1��1s22s22p63s23p63d104s1 ��1�֣� C ��2�֣�
��5��C2H2��g��+ 5/2O2��g�� = 2CO2��g��+ H2O��l�� ��H=-1300KJ/mol��3�֣�
�����������⿼�����ʽṹԪ�������ɣ�����Ԫ�������ڱ���λ�á������Ų������ԡ��������͡���������㡢�Ȼ�ѧ��Ӧ����ʽ�ȡ����ݽ��ʯ����Ȼ����Ӳ�����ʿ�֪TΪC����W���������2s22p3ΪN��W������⻯������Һ������Ϊ���Ӽ��γ����������Xԭ�ӵĵ�һ�����������ĵ��������ݿ�֪���ĵ�����ͻȻ���������4�����������3������ͬһ���Ӳ㣬����ԭ����������������ӣ����ԭ����������������֪������YΪS,Z��������Ϊ63-34=29��Ϊͭ����1��Nԭ�ӵ�p�ܼ��ǰ������Ϊ�ȶ��ṹ����һ�����ܱ�O�ߡ���2��CS2�ṹΪS =C=S����2���Ҽ�����3�����ʯ��ԭ�Ӿ��壬���AlN��ԭ�Ӿ��壬�����Ӽ��γɷ��Ӽ��γ���������������Һ������4�����ݷ�ӦCu��HCl��O2��CuCl��HO2����֪HO2�ǻ�ԭ���HO2�������ᣩ��һ�����ᣬ������ɷ�Ӧ�����c����5���þ�����4����8��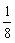 +6��
+6��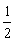 =4��Cuԭ�ӣ���������Ϊ
=4��Cuԭ�ӣ���������Ϊ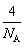 ��64g���辧���߳�Ϊx����x3��9��00=
��64g���辧���߳�Ϊx����x3��9��00=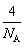 ��64g,x3=4��7��10-23��x=3��61��10-8cm�� ������ļ۵��Ӷ�Ϊ
��64g,x3=4��7��10-23��x=3��61��10-8cm�� ������ļ۵��Ӷ�Ϊ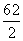 ��4������Ϊ��������ṹ������ԭ����ԭ��Ϊsp3�ӻ���
��4������Ϊ��������ṹ������ԭ����ԭ��Ϊsp3�ӻ���


 ��ʱѵ���������������ϵ�д�
��ʱѵ���������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������ABn������ԭ��A��û�й¶Ե��ӣ����ü۲���ӶԻ������ۣ�����˵����ȷ����(����)
A����n��2������ӵ�����ṹΪV��
B����n��3������ӵ�����ṹΪ������
C����n��4������ӵ�����ṹΪ����������
D������˵��������ȷ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ж����и�ʴ�ԣ�ʹ��ʱ����������Ƥ���ϣ�������ϴ�ӵ��Լ���
A���ƾ� B��NaHCO3��Һ C��65�����ϵ�ˮ D����ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ӵĹ�ҵ��ˮ����������ͼ��ͼ��ʾ��
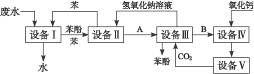
��1������������豸���н��е���_________��������д�������ƣ���ʵ��������һ������������__________________����д�������ƣ����С�
��2�����豸������豸�������A��_________�����豸������豸��������B��_________��
��3�����豸���з�����Ӧ�Ļ�ѧ����ʽΪ��_______________________________________��
��4�����豸���У�����B��ˮ��Һ��CaO��Ӧ������NaOH��H2O��_________��ͨ������________________����д�������ƣ�������ʹ��������롣
��5��ͼ�У���ѭ��ʹ�õ�������C6H6��CaO��________________��________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ���ǣ� ��
A�����ơ��ء�﨣����ֵ����У�卑��۵����
B������صĻ�ѧ��Ӧԭ����������ԭ��Ӧ�������ʹ�ŵ�ʱ��������ԭ��Ӧ������У�ȼ�ϵ�ص����������ʿɴ�100%
C����ѧ������ʹ�������ϣ�Ҳ����ʹԭ������
D��������-12��CF2Cl2��������ͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1����ҵ��������һ����Ҫ��Ӧ�ǣ�CO(g)+H2O(g) CO2(g)+ H2(g)
CO2(g)+ H2(g)
��֪��25��ʱ����1��C��ʯī��+1/2O2(g)=CO(g) ��H1=��111kJ/mol
��2��H2��g��+1/2O2(g)=H2O(g) ��H2=��242kJ/mol
��3��C��ʯī��+O2(g)=CO2(g) ��H3=��394kJ/mol
�Լ���25��ʱһ����̼��ˮ����ת��Ϊ�����Ͷ�����̼��Ӧ�ķ�Ӧ�� ��
��2����֪������Ӧ��427�� ʱ��ƽ�ⳣ����9.4�������Ӧ��ʼʱ��һ����̼��ˮ������Ũ�ȶ���0.01 mol/L������һ����̼�ڴ˷�Ӧ�����µ�ת���� ��������3λ��Ч���֣���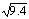 ��3.07��
��3.07��
��3�����ڻ�ѧ��Ӧ������Ҳ���о�����Ҫ���ݡ���һ�ܱ������г���1mol H2��1mol I2��ѹǿΪp(Pa) ������һ���¶���ʹ�䷢����Ӧ��H2(g)+I2(g)  2HI(g) ��H<0���ﵽƽ��������ܼӿ췴Ӧ���ʵ��ǣ� ��
2HI(g) ��H<0���ﵽƽ��������ܼӿ췴Ӧ���ʵ��ǣ� ��
�ٱ��������ݻ����䣬�����м���1mol H2��
�ڱ��������ݻ����䣬�����м���1mol N2��N2���μӷ�Ӧ����
�۱�������������ѹǿ���䣬�����м���1mol N2��N2���μӷ�Ӧ����
�ܱ�������������ѹǿ���䣬�����м���1mol H2��1mol I2��
�������ʼ�ķ�Ӧ�¶ȡ�
��4��2.0 mol PCl3��1.0molCl2�������������ܱ������У���һ�������·���������Ӧ��
PCl3(g)+ Cl2(g) PCl5(g)����ƽ��ʱ��PCl5Ϊ0.40mol�������ʱ����1.0 mol PCl3��0.5molCl2������ͬ�¶����ٴ�ƽ��ʱPCl5�����ʵ����ǣ� ��
PCl5(g)����ƽ��ʱ��PCl5Ϊ0.40mol�������ʱ����1.0 mol PCl3��0.5molCl2������ͬ�¶����ٴ�ƽ��ʱPCl5�����ʵ����ǣ� ��
A��0.4 mol B��0.2 mol C����0.2 mol D������0.2 mol����0.4 mol
��5����֪25���£�������Һ�д���������ϵ��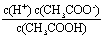 =1.75��10-5���е���ֵ�Ǹ��¶��´���ĵ���ƽ�ⳣ�������������ʼŨ��Ϊ0.010 mol/L��ƽ��ʱc(H+)= . ��
=1.75��10-5���е���ֵ�Ǹ��¶��´���ĵ���ƽ�ⳣ�������������ʼŨ��Ϊ0.010 mol/L��ƽ��ʱc(H+)= . ��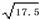 ��4.18��
��4.18��
����ʾ������ĵ��볣����С��ƽ��ʱ��c(CH3COOH)�ɽ�����Ϊ�Ե���0.010 mol/L��
��6����������Һ����μ���Ba(OH)2��Һ����������Ӹպó�����ȫʱ����Һ��pH 7����<��>��=���� ���ӷ�Ӧ�ܷ���ʽΪ ��
��������Һ����μ���Ba(OH)2��Һ�������Ӹպó�����ȫʱ����Һ��pH 7����<��>��=���� ���ӷ�Ӧ�ܷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��FeCl3��CuCl2�����Һ�У�����һ��������м����Ӧ��ȫ�����˳�������˵������ȷ���� (����)
A�����˳��Ĺ�����ֻ��ͭ������Һ��һ�����е���������Fe2����һ������Cu2��
B�����˳��Ĺ�����ֻ��ͭ������Һ��һ�����е���������Fe2�������ܺ�Cu2����Fe3��
C�����˳��Ĺ�����ֻ��ͭ������Һ��һ�����е���������Fe3����Fe2����һ������Cu2��
D�����˳��Ĺ����к�������ͭ������Һ��һ�����е���������Fe2����һ������Cu2����Fe3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪����100��ʱ����ˮ��c(H+)Ϊ1��10��6����ʱ��pH��12��NaOH��ҺV1 L��pH��l��H2SO4��ҺV2 L��ϣ������û����Һ��pH��10����V1��V2Ϊ��
A��1��9 B��10��1 C��9��1 D��1��10
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com