
请参照物质的溶解度表回答下列问题:
(1)写出制取过程中反应的化学方程式。
(2)若提供100 g水,则需NaOH的物质的量为多少?
(3)简述实验的操作过程。
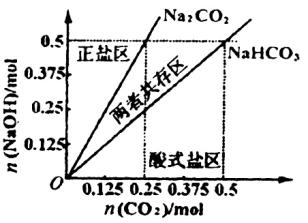
(4)在右图中反映上述实验过程的图象中,标出A点(即当![]() =
=![]() ,且n(
,且n(![]() )=0.125 mol时)的位置,并判断此时所得盐的组成及其物质的量。
)=0.125 mol时)的位置,并判断此时所得盐的组成及其物质的量。
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:022
用NaOH(s)、水、大理石和盐酸制取33 g纯NaHCO3。
请参照物质的溶解度表回答下列问题:
(1)写出制取过程中反应的化学方程式。
(2)若提供100 g水,则需NaOH的物质的量为多少?
(3)简述实验的操作过程。
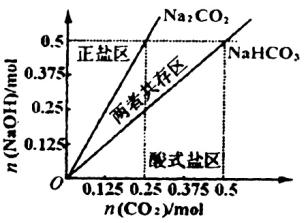
(4)在右图中反映上述实验过程的图象中,标出A点(即当![]() =
=![]() ,且n(
,且n(![]() )=0.125 mol时)的位置,并判断此时所得盐的组成及其物质的量。
)=0.125 mol时)的位置,并判断此时所得盐的组成及其物质的量。
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
(1)写出制取过程中反应的化学方程式。
(2)若提供100 g水,则需NaOH的物质的量为多少?
(3)简述实验的操作过程。
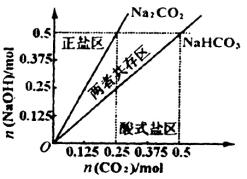
(4)在右图中反映上述实验过程的图象中,标出A点(即当![]() =
=![]() 且n(
且n(![]() )=)0.125 mol时)的位置,并判断此时所得盐的组成及其物质的量。
)=)0.125 mol时)的位置,并判断此时所得盐的组成及其物质的量。
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃ | 溶解度 |
NaHCO3 | 9 |
Na2CO3 | 33 |
NaOH | 110 |
(1)若用水100 g,则制取时需NaOH________________g。
(2)若用NaOH(s)17.86 g,则需用水_______________________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
参照下表几种物质的溶解度,用固体NaOH、水、CaCO3(s)、盐酸为原料制取33 g纯NaHCO3晶体。
| 25 ℃时溶解度/g | |
| NaHCO3 | 9 |
| Na2CO3 | 33 |
| NaOH | 110 |
(1)若用水100 g,则制取时需NaOH g。
(2)若用NaOH(s)17.86 g,则需用水 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com