
����Ŀ���ϳɰ���ӦΪ N2(g)+3H2(g) ![]() 2NH3(g)��H=+92.4kJmol��1������˵����ȷ����( ��
2NH3(g)��H=+92.4kJmol��1������˵����ȷ����( ��
A��һ�������£���N2������������N2�ķֽ��������ʱ���÷�Ӧ����ƽ��״̬
B��ȡ1mol N2��3mol H2�����ܱ������ڷ�Ӧ��ƽ��ʱ������2 mol NH3
C��һ�������·�Ӧ�ﵽƽ�⣬�ٳ���N2��������Ӧ���������淴Ӧ���ʼ�С
D��һ�������·�Ӧ�ﵽƽ�⣬�������¶ȣ���Ӧ��������ƽ��������Ӧ�����ƶ�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ƿ�����ȣ�Ũ�ȶ���1mol��L-1��������Һ�������������������һ�룻�����м���������CH3COONa������������������������������κθı䡣���Է�̪��ָʾ������NaOH��Һ�ζ�����������Һ������NaOH��Һ�����Ϊ
A. ��=��>�� B. ��>��>�� C. ��=��>�� D. ��=��=��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͬ�����£�1���X2��������3���Y2����������2���Z����������Z�Ļ�ѧʽΪ( )
A��XY3 B��XY C��X2Y D��X3Y2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״�����Ҫ�Ļ�ѧ��ҵ����ԭ�Ϻ�Һ��ȼ�ϡ���ҵ�Ͽ�����CO��CO2������ȼ�ϼ״�����֪�״��Ʊ����йػ�ѧ��Ӧ�Լ��ڲ�ͬ�¶��µĻ�ѧ��Ӧƽ�ⳣ�����±���ʾ��
��ѧ��Ӧ | ƽ�ⳣ�� | �¶�(���� | |
500 | 800 | ||
��2H2(g��+CO(g�� | K1 | 2.5 | 0.15 |
��H2(g��+CO2(g�� | K2 | 1.0 | 2.50 |
��3H2(g��+CO2(g�� | K3 | ||
��1��ij�¶��·�Ӧ����H2��ƽ��ת����(a������ϵ��ѹǿ(P���Ĺ�ϵ��ͼ��ʾ����ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ��K(A�� K(B��(����������������������������

��2����Ӧ���� (������������������������Ӧ��
��3���жϷ�Ӧ�ۡ�H 0����S 0(����>����=������<����
��500����2L���ܱ������У����з�Ӧ�������ijʱ��H2��CO2�� CH3OH��H2O�����ʵ����ֱ�Ϊ6mol��2 mol��10 mol��10 mol����ʱv(���� v(���� (����>����=������<����
��4��һ���¶��£���3 L�ݻ��ɱ����ܱ������з�����Ӧ������֪c(CO���뷴Ӧʱ��t�仯��������ͼ��ʾ������t0ʱ�̷ֱ�ı�һ����������������Ϊ����������������

����������Ϊ������ʱ���ı�������� ��
����������Ϊ������ʱ���ı�������� ��
��5��һ���¶��£�C(s����ˮ�������ܱ������У�����ƽ��״̬��C(s��+H2O(g��![]() CO(g��+H2(g������H>0��
CO(g��+H2(g������H>0��
��ƽ��ʱ��������ƽ����Է�������Mr(ƽ����ȡֵ��ΧΪ__________>Mr(ƽ��>__________��
����ʹ��CO��H2���淴Ӧ��������ͬ�¶��½���ƽ�⣬��ƽ���������ƽ����Է�������M��r(ƽ����ȡֵ��ΧΪ__________>M��r(ƽ��>__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��Ϊ����ȡ��̽���������ʣ�������װ��(���ּг�װ������ȥ)����ʵ�顣 [��ȡ�����ķ�Ӧԭ���� 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O]
CaCl2+2NH3��+2H2O]
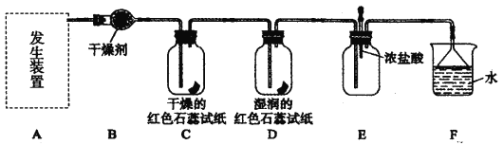
��ʵ��̽����
(1) ��������ԭ����ʵ������ȡ����Ӧѡ����ͼ��_______����װ�ý���ʵ�顣

(2)B װ���еĸ������ѡ��________( ���ʯ�ҡ���Ũ���ᡱ)��
(3)�� 5.35 g NH4Cl ���������� Ca(OH)2 ��Ӧ�������Ƶñ�״���°��������Ϊ_________L��( NH4Cl ��Ħ������Ϊ 53.5 g��mol��1)
(4)����ͨ�� C��D װ��ʱ����ֽ��ɫ�ᷢ���仯���� __________( �C����D��)��
(5)��ʵ�����һ��ʱ���ѹEװ���еĽ�ͷ�ιܣ�����1��2 ��Ũ���ᣬ�ɹ۲쵽��������__________��
(6)Fװ���е���©�������� _____________��
(7)ijͬѧ�ð����͵μӷ�̪��ˮ����Ȫʵ�飬������ƿ�ڲ�����ɫ��Ȫ������˵����������___________����(�����)��
a����ԭ�� b����������ˮ c����ˮ��Ӧ���ɼ�������
(8)��������;�ܹ㡣����ð����������������� 8NH3 + 6NO2 =7N2 + 12H2O�÷�Ӧ�а�������________( ������ԡ���ԭ�ԡ�)�������оٳ���������һ����;__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����(����)
A. �ѻ�����������͵������͵IJ���������
B. Ӳ֬�������������Ӧ��õ�����Ҫ��Ʒ��Ӳ֬�����
C. �Ҵ����������������������о�������OH
D. ��2 mL���м���1 mL���CCl4��Һ���������ϲ���Ϻ�ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ��õ����������Һ��������������ռ���Һ��װ����ͼ��ʾ������������������Ϊ���Ե缫�����ͬ��ͬѹ�£�������������ҵ������ԼΪ2:1������˵������ȷ���ǣ� ��
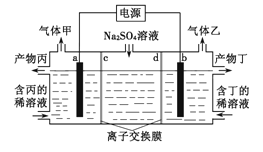
A��a�����Դ�ĸ�������
B�����ӽ���ĤdΪ�����ӽ���Ĥ
C�������Ϊ������Һ
D��a�缫��Ӧʽ��2H2O+2e��=H2��+2OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����(����)
A. ��ϩ��ʹ���Ը��������Һ��ɫ��������������Ӧ
B. ����һ������������Ũ���ᷴӦ�õ���������������ȡ����Ӧ
C. ��ȩ��һ��������������Ӧ�����Ҵ��������˻�ԭ��Ӧ
D. ��������Һ�м��뱥���������Һ����������ͭ��Һ���ᷢ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������������ԭ������������ ��
A����״����5.6L ���� B��4��ʱ9mLˮ
C��11gCO2 D��6.02��1022��H2SO4
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com