甲醇是一种可再生能源,具有广泛的开发和应用前景.
(l)已知在常温常压下反应的热化学方程式:
①CO ( g )+2H
2(g)?CH
3OH ( g )△H
1=-90kJ?mol
-1②CO ( g )+H
2O ( g )=CO
2 ( g )+H
2 ( g )△H
2=-41kJ?mol
-1写出由二氧化碳、氢气制备甲醇的热化学方程式:
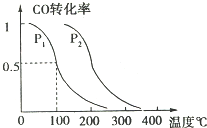
(2)在压强为0.1MPa 条件下.容积为VL 的容器中充入a mol CO 与2a mo1H
2 在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示;
①P
1
P
2 (填大于、小于或等于);
②在其它条件不变的情况下,再增加a mol CO 与2a mo1H
2,达到新平衡时,CO的转化率
(填“增大”、“减小”或“不变”,下同),平衡常数
.
(3)以甲醇为燃料的新型燃料电池,正极通入O
2,负极通入甲醇,在酸性溶液中甲醇与氧作用生成水和二氧化碳.该电池负极发生的反应是:CH
3OH+H
2O-6e
-=CO
2+6H
+①正极的电极反应式是
;放电时,H
+移向电池的
(填“正”或“负”)极;
②若以该燃料电池作为电源,用石墨作电极电解500mL 饱和食盐水,当两极共收集到标准状况下的气体1.12L(以不考虑气体的溶解)时,所得溶液的pH=
(假设反应前后溶液体积不变).

 甲醇是一种可再生能源,具有广泛的开发和应用前景.
甲醇是一种可再生能源,具有广泛的开发和应用前景.

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案