
【题目】在下列各溶液中,离子一定能大量共存的是( )
A.使甲基橙试液变红的溶液:![]() 、
、![]() 、
、![]() 、
、![]()
B.常温下,![]() 的溶液:
的溶液:![]() 、
、![]() 、
、![]() 、
、![]()
C.溶质为![]() 的溶液:
的溶液:![]() 、
、![]() 、
、![]() 、
、![]()
D.水电离出的![]() 的溶液:
的溶液:![]() 、
、![]() 、
、![]() 、
、![]()
科目:高中化学 来源: 题型:
【题目】碳、磷、硫等元素形成的单质和化合物在生活、生产中有重要的用途。
(1)下列氮原子的电子排布图表示的状态中,能量由低到高的顺序是____(填字母)。
A. ![]()
B. ![]()
C. ![]()
D. ![]()
(2)P4S3可用于制造火柴,其分子结构如图所示:
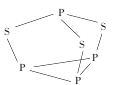
①P4S3分子中硫原子的杂化轨道类型为____。
②每个P4S3分子中含有的孤电子对的数目为____对。
(3)科学家合成了一种阳离子“N5n+”,其结构是对称的,5个N排成“V”形,每个N都达到8电子稳定结构,且含有2个氮氮三键,此后又合成了一种含有“N5n+”的化学式为“N8”的离子晶体(该晶体中每个N原子都达到了8电子稳定结构),N8的电子式为____。(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子的最外层均满足8电子稳定结构,其结构式为____。
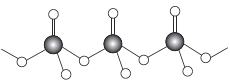
(4)直链多磷酸根阴离子是由两个或两个以上磷氧四面体通过共用顶角氧原子连接起来的,其结构如图所示。则由n个磷氧四面体形成的这类磷酸根离子的通式为____。
(5)碳酸盐中的阳离子不同,热分解温度就不同。下表为四种碳酸盐的热分解温度和对应金属阳离子的半径。随着金属阳离子半径的增大,碳酸盐的热分解温度逐渐升高,原因是 ___。
碳酸盐 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
热分解温度/℃ | 402 | 900 | 1172 | 1360 |
金属阳离子半径/pm | 66 | 99 | 112 | 135 |
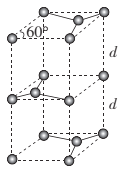
(6)石墨的晶胞结构如图所示。已知石墨的密度为ρg.cm-3,C-C键的键长为r cm,M为阿伏加德罗常数的值,则石墨晶体的层间距d= ___cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设 NA 为阿伏加德罗常数的值。下列说法正确的是
A.0.l mol C2H6O 分子中含 C-H 键数目为 0.5 NA
B.1 mol·L-1 的 NH4Cl 溶液中含有![]() 数目小于 0.1 NA
数目小于 0.1 NA
C.25℃时,1 L pH=13 的 Ba(OH)2 溶液中含有 OH-的数目为 0.2NA
D.1 mol Cl2 与足量铜铁合金反应,转移电子数一定是 2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将一小块钠放在石棉网上加热。回答下列问题:
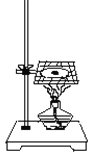
(1)观察到的实验现象有:____________________________________和黑色固体物质生成。
(2)产生以上现象的主要化学反应方程式为:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚砷酸(H3AsO3)可以用于治疗白血病,其在溶液中存在多种微粒形态,将KOH溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液的pH关系如图所示。下列说法正确的( )

A.人体血液的pH在7.35~7.45之间,用药后人体中含As元素的主要微粒是AsO33-
B.n(H3AsO3)∶n(H2AsO3-)=1∶1时,溶液显酸性
C.当pH调至11时发生反应的离子方程式是H3AsO3+OH-=H2AsO3-+H2O
D.pH=12时,溶液中c(H2AsO3-)+2c(HAsO32-)+3c(AsO33-)+c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下,H2和O2在Ag9(图中物质1)团簇上生成H2O2的吉布斯自由能(![]() )的部分变化曲线如图。下列说法错误的是( )
)的部分变化曲线如图。下列说法错误的是( )
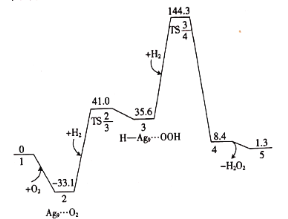
A.物质2中的O2是处于被吸附活化状态
B.物质3→物质4的过程中活化吉布斯自由能能垒为![]()
C.物质4可能为![]()
D.反应![]() 具有自发性
具有自发性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天门冬氨酸锌是一种补锌剂,可以![]() 、天门冬氨酸(
、天门冬氨酸(![]() )为原料制备。回答下列问题:
)为原料制备。回答下列问题:
(1)Zn成为阳离子时首先失去______轨道电子。碲(Te)与O同主族,则Te元素中电子占据的能量最高的能级是______。
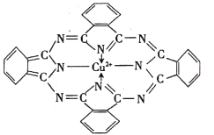
(2)P是N的同族元素,PH3与NH3中稳定性更高的是______(填化学式),其判断理由是______;酞菁铜可用于生产蓝色颜料(结构如图),其中C原子的轨道杂化类型为______。
(3)CO为______(填“极性”或“非极性”)分子。
(4)ZnO晶体的一种晶胞结构如图:
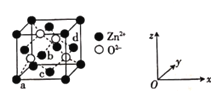
①![]() 的配位数为____________。
的配位数为____________。
②以晶胞边长为单位长度建立的坐标系可表示晶胞中锌原子的位置,称作原子分数坐标。图中原子a的分数坐标为![]() ,原子d的分数坐标为
,原子d的分数坐标为![]() ,则原子b和c的分数坐标分别为______、______。
,则原子b和c的分数坐标分别为______、______。
③设![]() 为阿伏加德罗常数的值。已知晶胞边长为
为阿伏加德罗常数的值。已知晶胞边长为![]() nm,则ZnO晶体的密度为______(列出计算式)
nm,则ZnO晶体的密度为______(列出计算式)![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)碳酸:H2CO3,K1=4.3×10﹣7,K2=5.6×10﹣11
草酸:H2C2O4,K1=5.9×10﹣2,K2=6.4×10﹣5
0.1mol/L Na2CO3溶液的pH_____0.1mol/L Na2C2O4溶液的pH;(选填“大于”“小于”或“等于”)
(2)等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是_____;若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是_____(选填编号);
a.c(H+)>c(HC2O![]() )>c(HCO
)>c(HCO![]() )>c(CO
)>c(CO![]() )
)
b.c(HCO![]() )>c(HC2O
)>c(HC2O![]() )>c(C2O
)>c(C2O![]() )>c(CO
)>c(CO![]() )
)
c.c(H+)>c(HC2O![]() )>c(C2O
)>c(C2O![]() )>c(CO
)>c(CO![]() )
)
d.c(H2CO3)>c(HCO![]() )>c(HC2O
)>c(HC2O![]() )>c(CO
)>c(CO![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作会引起实验结果偏高的是( )
A.测定硫酸铜晶体中结晶水含量的实验中,晶体加热完全失去结晶水后,将盛试样的坩埚放在实验桌上自行冷却
B.镀锌铁皮锌镀层厚度测量实验中,将铁皮用酒精灯持续加强热以彻底烘干
C.用标准碱滴定待测酸溶液时,装有标准碱的滴定管滴定前无气泡,滴定后有气泡
D.一定物质的量浓度的盐酸配制过程中用量筒量取计算所需的浓盐酸时,仰视观察刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com