
)单晶硅是信息产业中重要的基础材料。工业上可用焦炭与二氧化硅的混合物在高温下与氯气反应生成SiCl4和CO,SiCl4经提纯后用氢气还原得高纯硅。以下是实验室制备SiCl4的装置示意图。

实验过程中,石英砂中的铁、铝等杂质也能转化为相应氯化物,SiCl4、AlCl3、FeCl3遇水均易水解,有关物质的物理常数见下表:
物质 | SiCl4 | AlCl3 | FeCl3 |
沸点/℃ | 57.7 | - | 315 |
熔点/℃ | -70.0 | - | - |
升华温度/℃ | - | 180 | 300 |
请回答下列问题:
(1)写出装置A中发生反应的离子方程式:_____________, 装置D的硬质玻璃管中发生反应的化学方程式是????????????????????????? 。
(2)装置C中的试剂是?????????? ; D、E间导管短且粗的原因是????????????? 。
(3)G中吸收尾气一段时间后,吸收液中肯定存在OH-、Cl-和SO42-。请设计实验,探究该吸收液中可能存在的其他酸根离子(忽略空气中CO2的影响)。
【提出假设】假设1:只有SO32-;假设2:既无SO32-也无ClO-;假设3:?????? 。
【设计方案,进行实验】可供选择的实验试剂有:3 mol/L H2SO4、1 mol/L NaOH、0.01 mol/L KMnO4、溴水、淀粉-KI、品红等溶液。
取少量吸收液于试管中,滴加3 mol/L H2SO4至溶液呈酸性,然后将所得溶液分置于a、b、c三支试管中,分别进行下列实验。请完成下表:
序号 | 操? 作 | 可能出现的现象 | 结论 |
① | 向a试管中滴加几滴????????? 溶液 | 若溶液褪色 | 则假设1成立 |
若溶液不褪色 | 则假设2或3成立 | ||
② | 向b试管中滴加几滴????????? 溶液 | 若溶液褪色 | 则假设1或3成立 |
若溶液不褪色 | 假设2成立 | ||
③ | 向c试管中滴加几滴????????? 溶液 |
| 假设3成立 |
(1)MnO2+2Cl-+4H+ Mn2++Cl2↑+2H2O ;SiO2+2C+2Cl2
Mn2++Cl2↑+2H2O ;SiO2+2C+2Cl2 SiCl4+2CO
SiCl4+2CO
(2)浓硫酸;防止生成物中的AlCl3、FeCl3等杂质凝结成固体堵塞导管
(3)【提出假设】假设3:只有ClO-
【设计方案,进行实验】①溴水(或0.01 mol/L KMnO4溶液)②品红溶液;③淀粉-KI溶液;若溶液变为蓝色
【解析】
试题分析:(1)装置A中发生的反应是用高锰酸钾和浓盐水在加热的条件下制备氯气,其反应离子方程式MnO2+2Cl-+4H+ Mn2++Cl2↑+2H2O;氯气经过除杂后在D中和SiO2 与C在加热条件下进行反应生成SiCl4和CO,反应化学方程式SiO2+2C+2Cl2
Mn2++Cl2↑+2H2O;氯气经过除杂后在D中和SiO2 与C在加热条件下进行反应生成SiCl4和CO,反应化学方程式SiO2+2C+2Cl2  SiCl4+2CO(2)BC中分别为饱和食盐水和浓硫酸用来除去氯气中的HCl和水蒸气;石英砂中的铁、铝等杂质也能转化为相应氯化物,若导管较细使杂质凝结成固体堵塞导管(3)由假设1和假设2得知,要检测的为SO32-和ClO-,故假设3为只有ClO-;又因为SO32-会使KMnO4和溴水,并不与ClO-发生反应,故可以用来检测假设1,而均SO32-和ClO-具有漂白性,会使品红溶液褪色,故可以用来检测假设2;所有试剂中ClO-可以氧化KI使其生成I2,在淀粉溶液中显蓝色,可以用来检测假设3。
SiCl4+2CO(2)BC中分别为饱和食盐水和浓硫酸用来除去氯气中的HCl和水蒸气;石英砂中的铁、铝等杂质也能转化为相应氯化物,若导管较细使杂质凝结成固体堵塞导管(3)由假设1和假设2得知,要检测的为SO32-和ClO-,故假设3为只有ClO-;又因为SO32-会使KMnO4和溴水,并不与ClO-发生反应,故可以用来检测假设1,而均SO32-和ClO-具有漂白性,会使品红溶液褪色,故可以用来检测假设2;所有试剂中ClO-可以氧化KI使其生成I2,在淀粉溶液中显蓝色,可以用来检测假设3。
考点:化学方程式的书写;离子检验与化学实验操作


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:阅读理解

| 物质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | 57.7 | 12.8 | - | 315 | - |
| 熔点/℃ | -70.0 | -107.2 | - | - | - |
| 升华温度/℃ | - | - | 180 | 300 | 162 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
(15分)单晶硅是信息产业中重要的基础材料。通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硫、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450-500°C),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
![]()
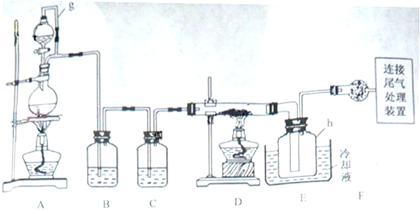
![]() 相关信息如下:
相关信息如下:
![]() a.四氯化硅遇水极易水解;
a.四氯化硅遇水极易水解;
![]() b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
![]() c.有关物质的物理常数见下表:
c.有关物质的物理常数见下表:
![]()

![]() 请回答下列问题:
请回答下列问题: www.ks5.u.com
www.ks5.u.com
![]() (1)写出装置A中发生反应的离子方程式 。
(1)写出装置A中发生反应的离子方程式 。
![]() (2)装置A中g管的作用是 ;装置C中的试剂是 ;装置E中的h瓶需要冷却理由是 。
(2)装置A中g管的作用是 ;装置C中的试剂是 ;装置E中的h瓶需要冷却理由是 。
![]() (3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的杂质元素是 (填写元素符号)。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的杂质元素是 (填写元素符号)。
![]() (4)为了分析残留物中铁元素的含量,先将残留物预处理,是铁元素还原成Fe2+ ,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:
(4)为了分析残留物中铁元素的含量,先将残留物预处理,是铁元素还原成Fe2+ ,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:
![]()
![]()
![]() ①滴定前是否要滴加指示剂? (填“是”或“否”),请说明理由 。
①滴定前是否要滴加指示剂? (填“是”或“否”),请说明理由 。
![]() ②某同学称取5.000g残留物,预处理后在容量瓶中配制成100ml溶液,移取25.00ml,试样溶液,用1.000×10-2mol? L-1KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00ml,则残留物中铁元素的质量分数是 。
②某同学称取5.000g残留物,预处理后在容量瓶中配制成100ml溶液,移取25.00ml,试样溶液,用1.000×10-2mol? L-1KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00ml,则残留物中铁元素的质量分数是 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年高三上学期化学一轮复习《从矿物到基础材料》专题综合测试(苏教版) 题型:实验题
单晶硅是信息产业中重要的基础材料。通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
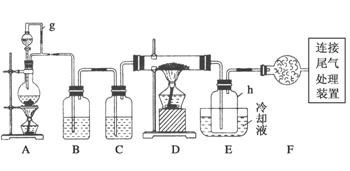
相关信息如下:
a.四氯化硅遇水极易水解;
b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
|
物质 |
SiCl4 |
BCl3 |
AlCl3 |
FeCl3 |
PCl5 |
|
沸点/℃ |
57.7 |
12.8 |
— |
315 |
— |
|
熔点/℃ |
-70.0 |
-107.2 |
— |
— |
— |
|
升华温度/℃ |
— |
— |
180 |
300 |
162 |
请回答下列问题:
(1)写出装置A中发生反应的离子方程式______________________。
(2)装置A中g管的作用是________;装置C中的试剂是________;装置E中的h瓶需要冷却的理由是__________________________________。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的杂质元素是________(填写元素符号)。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年重庆八中高三第二次月考理综试卷(化学部分) 题型:实验题
(16分)
单晶硅是信息产业中重要的基础材料。通常在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500 ℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
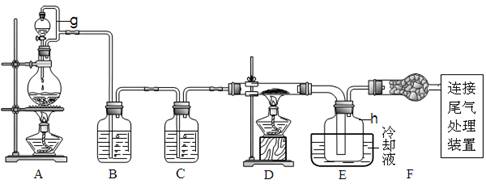
相关信息如下:
a.四氯化硅遇水极易水解;
b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
|
物质 |
SiCl4 |
BCl3 |
AlCl3 |
FeCl3 |
PCl5 |
|
沸点/℃ |
57.7 |
12.8 |
— |
315 |
— |
|
熔点/℃ |
-70.0 |
-107.2 |
— |
— |
— |
|
升华温度/℃ |
— |
— |
180 |
300 |
162 |
请回答下列问题:
(1)写出装置A中发生反应的离子方程式______________。
(2)装置A中g管的作用是______________;装置C中的试剂是____________;装置E中的h 瓶需要冷却的理由是______________。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的杂质元素是______________(填写元素符号)。
(4)为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:
5Fe2++MnO4-+8H+ =5Fe3++Mn2++4H2O
①滴定前是否要滴加指示剂?_________(填 “是”或“否”),请说明理由__________。
②某同学称取5.000g残留物后,所处理后在容量中瓶中配制成100 mL溶液,移取25.00 mL试样溶液,用1.000×10-2mol·L-1KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00 mL,则残留物中铁元素的质量分数是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com