
将5 mol/L的盐酸10 mL稀释到100 mL,再从中取出5 mL,这5 mL溶液的物质的量浓度为
| A.0.5 mol/L | B.0.25 mol/L | C.5 mol/L | D.1 mol/L |
科目:高中化学 来源: 题型:单选题
硫酸铜水溶液呈酸性,属保护性无机杀菌剂,对人畜比较安全,其与石灰乳混合可得“波尔多液”。实验室里需用180mL0.10mol·L-1的硫酸铜溶液,则应选用的容量瓶规格和称取溶质的质量分别为
| A.180mL容量瓶,称取2.88g硫酸铜 |
| B.200mL容量瓶,称取5.00g胆矾 |
| C.250mL容量瓶,称取6.25g胆矾 |
| D.250mL容量瓶,称取4.0g硫酸铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在NaCl、MgCl2两种盐配制的混合液中,Na+为0.2 mol,Mg2+为0.25 mol,
则Cl-为
| A.0.5 mol | B.0.6 mol | C.0.7 mol | D.0.8 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
甲、乙、丙是三种不含相同离子的可溶性强电解质。它们所含离子如下表所示:
| 阳离子 | NH4+、Na+、Mg2+ |
| 阴离子 | OH-、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体)。下列分析或结果错误的是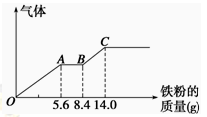
| A.原混合酸中NO3-物质的量为0.1 mol |
| B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.H2SO4浓度为2.5 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.2.3g金属钠与过量的氧气反应,无论是否加热与否转移电子数均为0.1NA |
| B.1mol Na2CO3晶体中含CO32-离子数小于NA |
| C.惰性电极电解食盐水,若线路中通过NA个电子,则阳极产生气体11.2L |
| D.0.1mol的CaO2中含阴离子数是0.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用NA表示阿伏加德罗常数的值,下列叙述中正确的是
| A.1mol氯气参加氧化还原反应,转移的电子数一定为2NA |
| B.在同温同压下,相同体积的任何气体单质所含的原子数目相同 |
| C.14 g乙烯和丙烯的混合物中总原子数为3NA个 |
| D.含2molH2SO4的浓硫酸与足量铜片在加热条件下反应,一定能产生NA个SO2气体分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用1L1mol·L-1NaOH溶液吸收0.8molCO2,所得溶液中Na2CO3和NaHCO3的物质的量之比约为( )
| A.1︰3 | B.1︰2 | C.2︰3 | D.3︰2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com