
某化学兴趣小组为了探究铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下。
编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
1 | Al、Mg | 稀盐酸 | 偏向Al |
2 | Al、Cu | 稀盐酸 | 偏向Cu |
3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
4 | Al、Mg | 氢氧化钠溶液 | 偏向Mg |
5 | Al、Zn | 浓硝酸 | 偏向Al |
试根据上表中的实验现象回答下列问题:
(1)实验1、2中Al所作的电极(正极或负极)是否相同(填“是”或“否”)? _______。
(2)对实验3完成下列填空:
①铝为___极,电极反应式: ______。
②石墨为____极,电极反应式: ________。
③电池总反应式: ____________。
(3)实验4中铝作负极还是正极____,理由是____。写出铝电极的电极反应式: _________。
(4)解释实验5中铝作正极的原因: __________。
(5)根据实验结果总结出影响铝在原电池中作正极或负极的因素: ________。
科目:高中化学 来源:2015-2016学年浙江省高二下期中化学试卷(解析版) 题型:选择题
使用前不需检查是否漏液的仪器是
A. 容量瓶 B. 分液漏斗 C. 酸式滴定管 D. 蒸馏烧瓶
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
标准状况下,两个体积相等的干燥圆底烧瓶中分别充满①NH3;②NO2进行喷泉实验。经充分反应后,瓶内溶液的物质的量浓度是( )
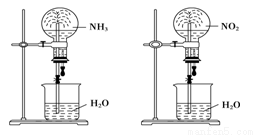
A.①=②
B.①<②
C.①>②
D.不能确定
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
同周期的IIA族元素与IIIA族元素核电荷数相差不可能是( )
A.1 B.11 C.17 D. 25
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆生产建设兵团二中高一下期中化学试卷(解析版) 题型:选择题
下列描述的化学反应状态,不一定是平衡状态的是
A.H2(g)+Br2(g) 2HBr(g) 恒温、恒容下,反应体系中气体的颜色保持不变
2HBr(g) 恒温、恒容下,反应体系中气体的颜色保持不变
B.2NO2(g)  N2O4(g) 恒温、恒容下,反应体系中气体的压强保持不变
N2O4(g) 恒温、恒容下,反应体系中气体的压强保持不变
C.CaCO3(s)  CO2(g)+CaO(s) 恒温、恒容下,反应体系中气体的密度保持不变
CO2(g)+CaO(s) 恒温、恒容下,反应体系中气体的密度保持不变
D.3H2(g)+N2(g)  2NH3(g) 反应体系中H2与N2的物质的量之比保持3∶1
2NH3(g) 反应体系中H2与N2的物质的量之比保持3∶1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆生产建设兵团二中高一下期中化学试卷(解析版) 题型:选择题
下列关于能量转换的认识中,不正确的是
A.电解水生成氢气和氧气时,电能转化为化学能
B.绿色植物进行光合作用时,太阳能转化为化学能
C.煤燃烧时,化学能主要转化为热能
D.白炽灯工作时,电能全部转化为光能
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二下期中化学试卷(解析版) 题型:推断题
A~G都是有机化合物,它们的转化关系如下:
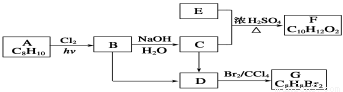
请回答下列问题:
(1)已知:6.0 g化合物E完全燃烧生成8.8 g CO2和3.6 g H2O;E的蒸气与氢气的相对密度为30,则E的分子式为__________。
(2)A为一取代芳香烃,B中含有一个甲基。由B生成C的化学方程式为_____________
(3)由B生成D、由C生成D的反应条件分别是____________、______________;
(4)由A生成B、由D生成G的反应类型分别是__________________、____________;
(5)F存在于栀子香油中,其结构简式为___________________;
(6)在G的同分异构体中,苯环上一硝化的产物只有一种结构的共有7种,其中核磁共振氢谱有两组峰,且峰面积比为1∶1的是____________________ (填结构简式)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省晋江市高一下学期期中考试化学试卷(解析版) 题型:实验题
某化学兴趣小组为探究元素性质的递变规律,设计可如下系列实验。
Ⅰ、(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,写出与盐酸反应最慢的金属发生反应的离子方程式___________________________________。
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:________________________________。
Ⅱ、利用下图装置可以验证非金属性的变化规律。
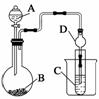 (加热及夹持仪器省略)
(加热及夹持仪器省略)
(3)实验室中提供药品浓硫酸、浓盐酸、Na2S、Na2SiO3、 MnO2、CaCO3,若要证明非金属性Cl>S;装置A、B、C中所装药品分别为_________________________________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_____________________________________。
(4)若要证明非金属性:S>C>Si,则A中加_________,B中加Na2CO3,C中加_________ ,则观察装置C中的实验现象为有白色沉淀生成。离子方程式为________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com