
| A、高炉炼铁 | B、生产水泥 | C、生产玻璃 | D、粗硅提纯 |
| ||
| ||


科目:高中化学 来源: 题型:
| A、垃圾是放错地方的资源,应分类回收利用 | B、加快化石燃料的开采与使用 | C、为改善食物的色、香、味并防止变质.可在其中加入大量食品添加剂 | D、为提高农作物的产量和质量,应大量使用化肥和农药 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
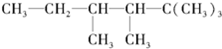
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑤不正确 | B、③④⑤不正确 | C、除④外其他都不正确 | D、都不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 叙述I | 叙述II |
| A | NaHCO3能与碱反应 | NaHCO3用作糕点的膨松剂 |
| B | 实验室常用MgSO4溶液与NaOH溶液制备Mg(OH)2沉淀 | Mg(OH)2不溶于强碱 |
| C | Cl2与Fe反应生成FeCl3 | 把FeCl3溶液直接蒸发结晶可以制备出FeCl3固体 |
| D | 铜丝与浓硫酸反应完,冷却后向试管中加入水来观察CuSO4溶液的蓝色 | 铜与浓硫酸反应生成了CuSO4和SO2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源:2015届广东省揭阳市高三上学期第一次阶段考试理综试卷(解析版) 题型:选择题
几种短周期元素的原子半径及主要化合价如下表:
元素代号 | X | Y | Z | M | N | R | Q | |
原子半径(×10-10 m) | 1.86 | 0.99 | 1.43 | 1.60 | 1.02 | 0.75 | 0.74 | |
主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +6 | +5 | —— |
最低负价 | —— | -1 | —— | —— | -2 | -3 | -2 | |
下列说法正确的是
A.气态氢化物的稳定性:N > Y
B.M(OH)2的碱性比XOH的碱性强
C.元素X和Q形成的化合物中可能含有共价键
D.X、Z、R的最高价氧化物对应的水化物之间可两两相互反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com