
| c(H+) |
| c(OH-) |
| A、C(B+)>C(A-)>C(OH-)>C(H+) |
| B、C(A-)>C(B+)>C(H+)>C(OH-) |
| C、C(B+)=C(A-)+C(HA) |
| D、C(B+)+C(H+)=C(A-)+C(OH-) |
| c(H+) |
| c(OH-) |
| c(H+) |
| c(OH-) |


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ? | ? |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
| A、2NaClO+CO2+H2O→Na2CO3+2HClO |
| B、HCN+Na2CO3→NaHCO3+NaCN |
| C、常温下电离常数:Ki2(H2CO3)>Ki(C6H5OH)>Ki(HCN) |
| D、结合质子能力的强弱顺序为:CO32-<HCO3-<CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 制取少量氨气 |
B、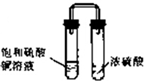 放置一段时间后,饱和硫酸铜溶液中出现蓝色晶体 |
C、 继续煮沸溶液至红褐色沉淀,停止加热,当光束通过体系时一定可产生丁达尔效应 |
D、 将海带灼烧成灰 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com