
W、Z、Y、X四种短周期元素的原子序数依次减少。W、Z位于同周期,原子半径Z大于W;Z、W的最高正价之和等于X的最高正价;W的质子数等于X、Y的质子数之和;W的最高价氧化物对应的水化物与Z、Y的最高价氧化物对应的水化物均能发生反应。下列说法中不正确的是
A. 气态氢化物的稳定性:X<Y
B. 没有X元素也就没有丰富的有机世界
C. 非金属性Y>X,金属性W>Z
D. 在一定条件下,利用X、Z或W单质的还原性,可以冶炼某些金属
科目:高中化学 来源: 题型:
A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,D、E、F为同一周期,A与D,C与F分别为同一主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)写出F在周期表中的位置________。画出D的离子结构示意图___________。
(2)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为_______________。
(3)C与F形成的常见化合物属于_________化合物(填“共价”或“离子”)。
(4)画出B单质的结构式_______________。科学家合成出了B元素形成的B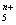 电子式
电子式 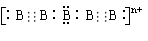 , 则n值为___ 。
, 则n值为___ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是
A.铁溶于稀硫酸中:2Fe+6H+=2Fe3++3H2↑
B.二氧化硫与足量烧碱溶液反应:S02+20H-=S032-+H20
C.醋酸溶液与氢氧化钠溶液反应:H++OH-=H20
D.浓盐酸与MnO2反应制Cl2:Mn02+2H++2C1- 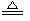 C12↑+Mn2++H20
C12↑+Mn2++H20
查看答案和解析>>
科目:高中化学 来源: 题型:
为说明氯比硫的非金属性强,下列事实可作依据的是
A、HCl的溶解性强于H2S B、氯的最高价为+7价
C、H2S中的S2-能被Cl2氧化 D、HClO的氧化性强于H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
同主族元素所形成的同一类化合物,其结构和性质往往相似,化合物PH4I是一种无色晶体,下列对它的描述中错误的是
A.它是共价化合物 B.在加热时,它能分解
C.它能跟碱发生反应 D.它可由PH3和HI化合而成
查看答案和解析>>
科目:高中化学 来源: 题型:
四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题。
| W | X | Y | Z | |
| 结构或性质 | 最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物 | 焰色反应呈黄色 | 在同周期主族元素形成的简单离子中,离子半径最小 | 最高正价与最低负价之和为零 |
(1)Z在元素周期表中位于________族。
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他三种物质发生化学反应,该元素是________(填元素符号)。
(3)①下列可作为比较X和Y金属性强弱的依据是________(填序号)。
a.自然界中的含量 b. 单质与酸反应时失去的电子数
c.单质与水反应的难易程度 d. 最高价氧化物对应水化物的碱性
②从原子结构的角度解释X的金属性强于Y的原因: ,原子半径X>Y,所以原子核对最外层电子的吸引力X<Y,失电子能力X>Y。
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与X的最高价氧化物对应的水化物的溶液混合,反应的化学方程式是____________________________________________________
(5)Y单质和Mg组成的混合物是一种焰火原料,某兴趣小组设计如下所示的实验方案,测定混合物中Y的质量分数。能确定混合物中Y的质量分数的数据有______________(填序号)。
a.m、n b.m、y c.n、y
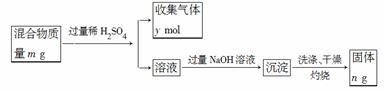 |
查看答案和解析>>
科目:高中化学 来源: 题型:
硼有两种天然同位素10B和11B,硼元素的相对原子质量为10.8,则10B与11B的物质的量之比为( )
A.1∶4 B.1∶2 C.1∶1 D.1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
有X、Y、Z三种短周期元素,X的气态氢化物化学式为H2X,此氢化物的分子量与X最高价氧化物的分子量之比为17:40,X原子核内质子数与中子数相等,Y与X可以形成离子化合物Y2X,Y的阳离子电子层结构与Ne相同,Z与X同周期,其气态单质是双原子分子,两原子共用1对电子。试回答:
(1)写出各元素符号:X 、Y 、Z 。
(2)X离子的结构示意图为 。X与Y形成的离子化合物的电子式为 , Z和氢形成的化合物的电子式为 。
(3)Y单质在空气中燃烧的化学方程式为 ,生成物与水反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下述实验设计能够达到目的的是
| 选项 | 实验目的 | 实验设计 |
| A | 证明Ksp(AgCl)﹥Ksp(AgI) | 往AgCl悬浊液中滴入几滴KI溶液 |
| B | 除去Cu粉中混有的CuO | 向混合物中滴加适量稀硝酸 |
| C | 检验溶液中是否含有Fe2+ | 向溶液中滴入氯水后,再滴加KSCN溶液 |
| D | 证明H2CO3酸性比H2SiO3强 | Na2CO3和SiO2在高温下熔融反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com