
| A. | CH2=CH-Cl | B. | CH≡CH | C. | 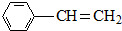 | D. | CH2=c(CH3)-CH=CH2 |
分析 在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行判断.
解答 解:A、乙烯为平面结构,CH2=CH-Cl中氯原子处于乙烯中H原子位置,所碳原子都处在同一平面上,故A不选;
B、CH≡CH为直线结构,所有原子可以都处在同一平面上,故B不选;
C、乙烯和苯是平面型结构,单键可以旋转,所以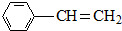 中所有原子有可能在同一个平面上,故C不选;
中所有原子有可能在同一个平面上,故C不选;
D、CH2=(CH3)-CH=CH2分子中的甲基是和甲烷具有相似的结构为空间四面体,所以原子不可能处于同一平面,故D选;
故选D.
点评 本题主要考查有机化合物的结构特点,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:解答题
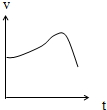 氯酸钾和亚硫酸氢钠发生氧化还原反应生成-1价的氯和+6价的硫 的速率如图所示,已知这个反应的速率除了与反应物浓度有关外,还随着溶液中c(H+)增大而加快
氯酸钾和亚硫酸氢钠发生氧化还原反应生成-1价的氯和+6价的硫 的速率如图所示,已知这个反应的速率除了与反应物浓度有关外,还随着溶液中c(H+)增大而加快查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Fe3+、Al3+、H+ | B. | Na+ | ||
| C. | Na+、Fe3+ | D. | Na+、Fe2+、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①表示化学反应H2(g)+Cl2(g)═2HCl(g)的能量变化,则该反应的反应热△H=+183 kJ/mol | |
| B. | ②表示其他条件不变时,反应4A(g)+3B(g)?2C(g)+6D在不同压强下B的体积分数随时间的变化,则D一定是气体 | |
| C. | ③表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 | |
| D. | ④表示10 mL 0.1 mol/L Na2CO3和NaHCO3两种溶液中,分别滴加0.1 mol/L盐酸,产生CO2的体积随盐酸体积的变化,则b表示Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 168 mL | B. | 224 mL | C. | 336 mL | D. | 504 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LH2O含有的分子数为NA | |
| B. | 常温常压下,17gNH3所含的原子数目为4NA | |
| C. | 1molNa2O2与H2O完全反应,转移2NA个电子 | |
| D. | 40gNaOH溶解在1L水中,得到的物质的量浓度为1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
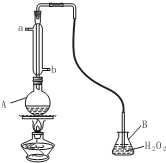 工业制硫酸尾气中的SO2,是一种空气污染物,同时也是一种重要的化工原料,采用氨吸收法进行循环利用,便可以变废为宝.
工业制硫酸尾气中的SO2,是一种空气污染物,同时也是一种重要的化工原料,采用氨吸收法进行循环利用,便可以变废为宝.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)随着温度升高而降低 | B. | 在35℃时,c(H+)>c(OH-) | ||
| C. | 蒸馏水中通HCl,Kw增大 | D. | 温度升高有利于水的电离 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com