
 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案科目:高中化学 来源: 题型:
下列关于有机物分子结构说法不正确的是( )
A.苯的邻位二溴代物只有一种能证明苯分子中不存在碳碳单、双键交替的排布
B.乙烯容易与溴水发生加成反应,且1 mol乙烯完全加成消耗1 mol溴单质能证明乙烯分子里含有一个碳碳双键
C.甲烷的一氯代物只有一种可证明甲烷为正四面体结构
D.1 mol乙醇与足量的钠反应生成0.5 mol氢气,可证明乙醇分子中只有一个羟基
查看答案和解析>>
科目:高中化学 来源: 题型:
准确称取某种铁的氧化物2.88 g,用足量的CO进行还原,将生成的CO2全部用足量的澄清石灰水吸收,得到沉淀4 g,则这种铁的氧化物为 ( )
A. Fe3O4 B.Fe2O3 C. FeO D.以上都不是
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
①铁能被磁铁吸引 ②在人体的血红蛋白中含有铁元素 ③镁在空气中可剧烈燃烧,并发出强光 ④铁能在氧气中剧烈燃烧,生成黑色的Fe3O4 ⑤在空气中加热铜可生成黑色的CuO
A.①②④⑤ B.②③④⑤ C.①③④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
某学校课外活动小组仅有一大一小两试管和氢氧化钠溶液。甲、乙两个同学找来铝制废牙膏皮,各自设计了一套装置如下图,制取并收集一试管氢气。
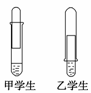
(1)哪个学生设计的装置比较合理?____(填“甲”或“乙”),另一设计装置不合理的原
因________________________________________________________________________
________________________________________________________________________。
(2)用比较合理的装置制取氢气,要使氢气充满收集氢气的试管,应该采取的措施是
________________________________________________________________________。
(3)还可以用哪些常见物品和试剂代替废牙膏皮和氢氧化钠溶液完成实验?
________________________________________________________________________
________________________________________________________________________。
(4)测定H2和空气混合气体的爆炸范围实验如下所述。取10支大试管,依次盛水90%(体积分数)、80%……再用排水集气法收集H2,而后分别把试管口移近酒精灯火焰,实验结果如下:
| H2体积分数/% | 90 | 80 | 70 | 60~20 | 10 | 5 |
| 空气体积分数/% | 10 | 20 | 30 | 40~80 | 90 | 95 |
| 点燃现象 | 安静 燃烧 | 安静 燃烧 | 弱爆炸 | 强爆炸 | 弱爆炸 | 不燃烧 不爆炸 |
由上述实验结果评价:用向下排空气法收集H2,保持试管倒置移近火焰,如果只发出轻微的“噗声”,表示收集的H2已纯净的说法的真正涵义:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于可逆反应2CO(g)+2NO(g)N2(g)+2CO2(g) ΔH<0,下列说法正确的是 ( )。
A.加入催化剂,平衡正向移动
B.在恒温、恒容条件下,加入氢氧化钠,平衡不移动
C.在恒温、恒压条件下,通入He气,平衡不移动
D.降温,平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
氨气是重要的化工原料
(1)已知: N2(g)+O2(g)=2NO(g) △H= +180.5kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H= -905kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H= -483.6kJ·mol-1
写出氨气在高温高压催化剂条件下生成氮气和氢气的热化学方程式: ;如果在1L密闭容器中,3mol NH3 在等温条件下充分反应,2min后达到平衡,平衡时的反应热为92.4kJ ,则在这段时间内v(H2)= ;保持温度不变,将起始NH3的物质的量调整为8mol,平衡时NH3的转化率为 。
(2)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式: ,
科学家利用此原理,设计成氨气一氧气燃料电池,则通入氨气的电极是 (填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为 。
(3)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是 (填字母代号)。
4NO(g)+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是 (填字母代号)。
a.增大压强 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
(4)如果某氨水的电离程度为1%,浓度为0.01 mol/LMgCl2溶液滴加氨水至开始产生沉淀时(不考虑溶液体积变化),溶液中的NH3·H2O的浓度为 {已知Ksp[Mg(OH)2]=4.0×10-12]}
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com