
下列与化学概念有关的说法正确的是
A.电解、电离的过程都需要消耗电能
B.元素的非金属性越强,对应单质的活泼性一定越强
C.有单质参加或生成的化学反应一定是氧化还原反应
D.只含共价键的物质不一定是共价化合物
科目:高中化学 来源:2013-2014山东省兰陵县下学期期中考试高二化学试卷(解析版) 题型:选择题
将0.1mol两种气态烃组成的混合气体完全燃烧后得3.36L(标准状况)CO2和3.6gH2O下列说法正确的是
A.一定有乙烯 B.一定有甲烷 C.可能有丙烯 D.可能有乙烷
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省乳山市下学期期中考试高一化学试卷(解析版) 题型:简答题
(8分)请用相关知识回答下列问题:
(1)用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,实验过程测得的CO2气体体积随时间变化如右图所示。
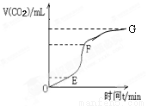
①________段化学反应速率最快,_______段收集的二氧化碳气体最多。
②除加入蒸馏水外,当加入下列物质中的 (填序号)时,则能够减缓上述反应的速率。
A.醋酸钠溶液 B.碳酸钙粉末 C.稀硫酸 D.浓盐酸
(2)原电池是一种能量装置。
①下列在理论上可用来设计原电池的反应是 (填序号)。
A.NaOH +HCl== NaCl+H2O B.2FeCl3+Cu=2FeCl2+CuCl2
NaCl+H2O B.2FeCl3+Cu=2FeCl2+CuCl2
C.CuSO4 +2NaOH== Cu(OH)2+Na SO4 D.C2H6O +3O2== 3H2O+2CO2
②实验室中用锌片与硫酸反应制取氢气时,向反应溶液中滴加几滴CuSO4溶液,可以发现产生氢气速率明显加快,其原因是 。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省乳山市下学期期中考试高一化学试卷(解析版) 题型:选择题
国外科学家曾将铅(Pb)和氪(Kr)两种元素的原子核对撞,获得了一种质子数为118、
质量数为293的新元素,该元素原子核内的中子数和核外电子数之差为
A.47 B.57 C.61 D.175
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省临沂市高三三模试卷理科综合化学试卷(解析版) 题型:选择题
下列有关实验操作、现象或原理均正确的是
选项 | 实验操作 | 实验现象或原理 |
A | 将海带灼烧,加水浸泡后过滤,向滤液中加入CCl4,振荡后静置 | 液体分层,下层显紫红色 |
B | 向氢氧化铝胶体中逐滴加入稀盐酸或氢氧化钠稀溶液 | 均先出现沉淀后溶解 |
C | 将40.0gNaoH固体溶于1.0L蒸馏水中配成溶液 | NaOH的物质的量浓度为1.0mol/L |
D | 向BaSO4饱和溶液中加入饱和Na2CO3溶液 | 有白色沉淀产生,说明Ksp(BaSO4)大于Ksp(BaCO3) |
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省临沂市高三5月二模理综化学试卷(解析版) 题型:填空题
(17分)金属镍具有优良的物理和化学特性,是高技术产业的重要原料。
(1)羰基法提纯镍涉及的反应为:Ni(s)+4CO(g) Ni(CO)4(g)
Ni(CO)4(g)
①当温度升高时, 减小,则?H 0(填“>”或“<”)。
减小,则?H 0(填“>”或“<”)。
②一定温度下,将一定量的粗镍和CO加入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________(填代号)。

若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数 (填“增大”、“不变”或“减小”),反应进行3s后测得Ni(CO)4的物质的量为0.6mol,则0—3s内的平均反应速率v(CO)=____mol 。
。
③要提高上述反应中CO的转化率,同时增大反应速率,可采取的措施为____________________(写出一条措施即可)。
(2)以NiS04溶液为电解质溶液进行粗镍(含Fe、Zn、Cu、Pt、Au等杂质)的电解精炼,下列说法正确的是____________(填代号)。(已知氧化性: )
)
a.电解过程中,化学能转化为电能
b.粗镍作阳极,发生还原反应
c.利用阳极泥可回收Cu、Pt、Au等金属
d.粗镍精炼时通过的电量与阴极析出镍的质量成正比
(3)工业上用硫化镍(NiS)作为电极材料冶炼镍。电解时,硫化镍中的硫元素以单质形态沉积在某电极附近,镍元素以Ni2+形态进入电解液中,如图所示。硫化镍与电源的____________(填“正极”或“负极”)相接。写出阳极的电极反应式________________。

查看答案和解析>>
科目:高中化学 来源:2013-2014山东省临沂市高三5月二模理综化学试卷(解析版) 题型:选择题
生活中的某些问题常常涉及化学知识,下列叙述错误的是
A.纯碱可用于制造玻璃,也可用于除去物品表面的油污
B.用聚氯乙烯代替木材生产包装盒、快餐盒等,以减少木材的使用
C.黄河人海口沙洲的形成和卤水点豆腐,都体现了胶体聚沉的性质
D.“煤改气”、“煤改电”等燃料改造工程有利于减少环境污染
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省下学期高二期末化学模拟试卷(解析版) 题型:选择题
进行一氯取代后,只生成三种沸点不同的产物的烷烃是
A.(CH3)2CHCH2CH2CH3 B.(CH3CH2)2CHCH3
C.(CH3)2CHCH(CH3)2 D.(CH3)3CCH2CH3
查看答案和解析>>
科目:高中化学 来源:2013-2014安徽省皖南八校高三第三次联考理综化学试卷(解析版) 题型:填空题
(15分)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增加。相关信息如下表所示,根据推断回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
A | A的最高价氧化物对应的水化物化学式为H2AO3 |
B | B元素的第一电离能比同周期相邻两个元素都大 |
C | C原子在同周期原子中半径最大(稀有气体除外),其单质焰色为黄色 |
D | Z的基态原子最外层电子排布式为3s23p2 |
E | E与C位于不同周期,E原子核外最外层电子数与C相同,其余各层电子均充满 |
(1)C在周期表中位于第 周期第 族,E基态原子核外电子排布式是
(2)A、B、D三种元素电负性由大到小排列顺序为 ,其中A的最高价氯化物构成晶体的微粒间作用力为
(3)A和B的最简单氢化物中较稳定的是 (填化学式)。B的最简单氢化物和E的黑色氧化物固体在加热时可反应,写出其反应方程式
(4)E的单质和过氧化氢在稀硫酸中可反应,有人将这个反应设计成原电池,请写出正极反应方程式
(5)煤燃烧产生的烟气中有B的氧化物,会引起严重的环境问题,因此,常用AH4催化还原以消除污染,已知:
① AH4(g)+2 BO2(g)= B2(g)+AO2(g)+2H2O (g) △H1=-867kJ/mol
② 2BO2(g) ? B2O4(g) △H2=-56.9 kJ/mol
写出AH4和B2O4反应的热化学方程式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com