
| 序号 | 试验内容 | 试验结果 |
| 1 | 加AgNO3溶液 | 有白色沉淀生成 |
| 2 | 加足量NaOH溶液并加热 | 收集到气体1.12L(已折算成标准状况下的体积) |
| 3 | 加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.27g 第二次称量读数为2.33g |
| 阴离子符合 | 物质的量浓度(mol?L-1) |
| ______ | ______ |
| ______ | ______ |
| ______ | ______ |
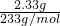 =0.01mol,BaCO3为6.27g-2.33g═3.94g,物质的量为
=0.01mol,BaCO3为6.27g-2.33g═3.94g,物质的量为 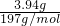 =0.02mol.
=0.02mol. =0.1mol/L,
=0.1mol/L,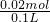 =0.2mol/L,
=0.2mol/L,| 阴离子符号 | 物质的量浓度(mol?L-1) |
| CO32- | 0.2mol?L-1 |
| SO42- | 0.1mol?L-1 |
 计算溶液中含有的离子浓度.
计算溶液中含有的离子浓度.

 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
+ 4 |
2- 3 |
2- 4 |
| 实验 序号 |
实验内容 | 实验结果 |
| 1 | 加AgNO3溶液 | 有白色沉淀生成 |
| 2 | 加足量NaOH溶液并加热 | 收集到气体1.12L(已折算成标准状况下的体积) |
| 3 | 加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.27g,第二次称量读数为2.33g |
| 阴离子符号 | 物质的量浓度(mol/L) | ||||
SO
SO
|
0.1 0.1 | ||||
CO
CO
|
0.2 0.2 | ||||
+ 4 |
2- 3 |
2- 4 |
+ 4 |
2- 3 |
2- 4 |
+ 4 |
2- 3 |
2- 4 |
+ 4 |
2- 3 |
2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、![]() 、Mg2+、Ba2+、CI-、
、Mg2+、Ba2+、CI-、 ![]() 、
、 ![]() 。将该混合物溶于水后得澄清溶液。现取3份l00mL该溶液分别进行如下实验:
。将该混合物溶于水后得澄清溶液。现取3份l00mL该溶液分别进行如下实验:
| 试验序号 | 试验内容 | 试验结果 |
| ||
| 1 | 加AgNO3溶液 | 有白色沉淀生成 |
| ||
| 2 | 加足量NaOH溶液并加热 | 收集到气体1.12L(已折算成 |
| ||
| 标准状况下的体积) |
| ||||
| 3 | 加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然 后干燥、称量 | 第一次称量读数为6.27g,第 二次称量读数为2.33g |
| ||
试回答下列问题:
(1)根据实验1对Cl-是否存在的判断是 (填“一定存在”、“一定不存在”或“不能确定”);根据实验l~3判断混合物中一定不存在的离子是 。
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满):
| 阴离子符号 | 物质的量浓度(mo1·L-) | |
(3)试确定K- 是否存在? ,判断的理由是
。
查看答案和解析>>
科目:高中化学 来源:2013届内蒙古巴彦淖尔市一中高三9月月考化学试卷(带解析) 题型:填空题
(18分)由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、Cl-、NH4+、Mg2+、Ba2+、CO32—、SO42—。将该混合物溶于水后得澄清溶液,现取三份100 mL该溶液分别进行如下实验:
| 实验序号 | 实验内容 | 实验结果 |
| 1 | 加AgNO3溶液 | 有白色沉淀生成 |
| 2 | 加足量NaOH溶液并加热 | 收集到气体1.12 L(已折算成标准状况下的体积) |
| 3 | 加足量BaCl2溶液,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.27 g,第二次称量读数为2.33 g。 |
| 阴离子符号 | 物质的量浓度(mol·L-1) |
| | |
| | |
查看答案和解析>>
科目:高中化学 来源:2010年广东省深圳高级中学高三上学期第一次月考化学试题 题型:填空题
(10分)由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、NH4+、Mg2+、Cu2+、Ba2+、C1—、SO42—、CO32-。将该混合物溶于水后得无色澄清溶液,现分别取3份100mL该溶液进行如下实验:
| 实验序号 | 实验内容 | 实验结果 |
| a | 加AgNO3溶液 | 有白色沉淀生成 |
| b | 加足量NaOH溶液并加热 | 收集到气体1.12L(已折算成标准 状况下的体积) |
| c | 加足量BaC12溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 | 第一次称量读数为6. 27g,第二次 称量读数为2.33g |
查看答案和解析>>
科目:高中化学 来源:2012年鲁科版高中化学选修6 3.1 物质组分的检验练习卷(解析版) 题型:填空题
由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、Cl-、NH4+、Mg2+、CO32-、Ba2+、SO42-。将该混合物溶于水后得澄清溶液,现取3份100 mL该溶液分别进行如下实验:
|
实验序号 |
实验内容 |
实验结果 |
|
1 |
加AgNO3溶液 |
有白色沉淀生成 |
|
2 |
加足量NaOH溶液并加热 |
收集到气体1.12 L(已折算成标准状况下的体积) |
|
3 |
加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 |
第一次称量读数为6.27 g,第二次称量读数为2.33 g |
试回答下列问题:
(1)根据实验1对Cl-是否存在的判断是________(填“一定存在”、“一定不存在”或“不能确定”);根据实验1~3判断混合物中一定不存在的离子是________。
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满):
|
阴离子符号 |
物质的量浓度/mol·L-1 |
|
|
|
|
|
|
(3)试确定K+是否存在?________,判断的理由是
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com