
有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 |
|
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,仅有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,只有A中放出无色气体,只有C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、D的化学式:B ,D 。
(2)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物化学式为 。
(3)C常用作净水剂,用离子方程式表示其净水原理 。
(4)在A溶液中加入少量澄清石灰水,其离子方程式为 。
(5)向20 mL 2 mol·L-1C溶液中加入30 mL E溶液,充分反应后得到0.78 g沉淀,则E溶液的物质的量浓度可能是 mol·L-1。
由①知D中含Cu2+,由④知D中含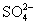 ,故D为CuSO4;由②知C中含Al3+,由③知C中含K+,由④知C中还含
,故D为CuSO4;由②知C中含Al3+,由③知C中含K+,由④知C中还含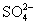 ,故C为KAl(SO4)2;由②知E中含OH-,结合③可判断出E为NaOH;由④知A中含
,故C为KAl(SO4)2;由②知E中含OH-,结合③可判断出E为NaOH;由④知A中含 ,结合③可判断A为NaHCO3;B中含K+,由④知B中不含
,结合③可判断A为NaHCO3;B中含K+,由④知B中不含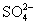 ,结合⑤可判断B只能为KNO3。
,结合⑤可判断B只能为KNO3。
(2)等物质的量的NaHCO3和NaOH在溶液中恰好反应:NaHCO3+NaOH====Na2CO3+H2O得Na2CO3溶液,将Na2CO3溶液蒸干得溶质Na2CO3。
(3)KAl(SO4)2在水中电离出Al3+,Al3+水解生成的Al(OH)3胶体能吸附水中的悬浮杂质形成沉淀,所以KAl(SO4)2可作净水剂。
(4)根据离子方程式书写的“以少定多”原则,可写出该反应的离子方程式。
(5)若NaOH不足,n(NaOH)=3n[Al(OH)3]=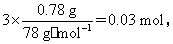
c(NaOH)=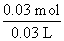 =1 mol·L-1;若NaOH过量,完全沉淀Al3+消耗NaOH的物质的量为3×2 mol·L-1×0.02 L=0.12 mol,溶解Al(OH)3沉淀消耗NaOH的物质的量为0.03 mol,故c(NaOH)=
=1 mol·L-1;若NaOH过量,完全沉淀Al3+消耗NaOH的物质的量为3×2 mol·L-1×0.02 L=0.12 mol,溶解Al(OH)3沉淀消耗NaOH的物质的量为0.03 mol,故c(NaOH)=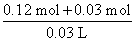 =5 mol·L-1。
=5 mol·L-1。
答案:(1)KNO3 CuSO4 (2)Na2CO3
(3)Al3++3H2O Al(OH)3(胶体)+3H+
Al(OH)3(胶体)+3H+
(4)2 +Ca2++2OH-====CaCO3↓+2H2O+
+Ca2++2OH-====CaCO3↓+2H2O+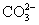 (5)1或5
(5)1或5
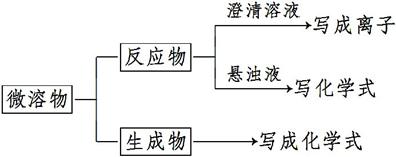
【方法技巧】书写离子方程式时微溶物及酸式盐的拆写原则
(1)微溶物:


科目:高中化学 来源: 题型:
乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明不正确的是( )
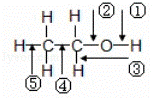
|
| A. | 和浓H2SO4共热至170℃时,键②和⑤断裂 |
|
| B. | 和乙酸共热发生酯化反应时,键②断裂 |
|
| C. | 在铜催化下和氧气反应时,键①和③断裂 |
|
| D. | 和氢卤酸共热时键②断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
根据反应 8NH3+3Cl2=6NH4Cl+N2 回答下列问题:
(1)氧化剂是,还原剂NH3.
(2)氧化剂与氧化产物的质量比.
(3)当有68g NH3参加反应时,计算被氧化的物质的质量.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的一组是( )
①不溶于水的盐(CaCO3、BaSO4等)都是弱电解质
②盐都是强电解质
③0.5 mol·L-1的所有一元酸中氢离子浓度都是0.5 mol·L-1
④强酸溶液中氢离子浓度一定大于弱酸溶液中氢离子浓度
⑤电解质溶液导电的原因是溶液中有自由移动的阴、阳离子
⑥熔融的电解质都能导电
A.①③⑤⑥ B.②④⑤⑥
C.只有⑤ D.只有⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的
是( )
A.0.1 mol·L-1NaOH溶液:K+、Na+、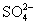 、
、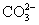
B.0.1 mol·L-1Na2CO3溶液:K+、Ba2+、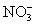 、Cl-
、Cl-
C.0.1 mol·L-1FeCl3溶液:K+、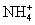 、I-、SCN-
、I-、SCN-
D.c(H+)/c(OH-)= 1×1014的溶液:Ca2+、Na+、ClO-、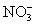
查看答案和解析>>
科目:高中化学 来源: 题型:
某离子晶体中,晶体结构最小的重复单元如图:A为阴离子,在正方体内,B为阳离子,分别在顶点和面心,则该晶体的化学式为( )

A.B2A B.BA2
C.B7A4 D.B4A7
查看答案和解析>>
科目:高中化学 来源: 题型:
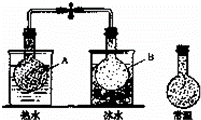
已知反应:2NO2 (g)⇌N2O4(g),把NO2、N2O4的混合气体盛装在两个连通的烧瓶里,然后用止水夹夹住橡皮管,把烧瓶A放入热水里,把烧瓶B放入冰水里,如图所示.与常温时烧瓶内气体的颜色进行对比发现,A烧瓶内气体颜色变深,B烧瓶内气体颜色变浅.下列说法错误的是( )
|
| A. | 上述过程中,A烧瓶内正、逆反应速率均加快 |
|
| B. | 上述过程中,B烧瓶内c(NO2)减小,c(N2O4)增大 |
|
| C. | 上述过程中,A、B烧瓶内气体密度均保持不变 |
|
| D. | 反应2NO2(g)⇌N2O4(g)的逆反应为放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g)+2B(g)⇌xC(g)△H=﹣192kJ•mol﹣1,向M、N中都通入1mol A和2mol B的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )

|
| A. | 若x=3,达到平衡后A的体积分数关系为:φ(M)>φ(N) |
|
| B. | 若x>3,达到平衡后B的转化率关系为:α(M)>α(N) |
|
| C. | 若x<3,C的平衡浓度关系为:c(M)>c(N) |
|
| D. | x不论为何值,起始时向N容器中充入任意值的C,平衡后N容器中A的浓度均相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com