
| A. | 在铁催化作用下,苯与溴水能发生取代反应 | |
| B. | 天然橡胶即聚2-甲基-1,3-丁二烯中含有大量碳碳双键,容易老化 | |
| C. | 有机物  的一氯代物有5种 的一氯代物有5种 | |
| D. | 乙酸乙酯、油脂分别与热NaOH溶液反应均是皂化反应 |
分析 A.苯与液溴反应,不与溴水反应;
B.天然橡胶中含有碳碳双键,能被空气中的氧气氧化;
C.该有机物具有对称结构,其分子中含有3种等效H;
D.乙酸乙酯与氢氧化钠溶液的反应不是皂化反应.
解答 解:A.在铁催化作用下,苯与液溴能发生取代反应,但不与溴水反应,故A错误;
B.聚2-甲基-1,3-丁二烯中含有大量碳碳双键,则天然橡胶受空气、日光作用会被氧化而老化,故B正确;
C. 分子中含有3种H原子,则其一氯代物有3种,故C错误;
分子中含有3种H原子,则其一氯代物有3种,故C错误;
D.皂化反应是油脂与氢氧化钠或氢氧化钾溶液混合发生水解,高级脂肪酸盐和甘油的反应,乙酸乙酯与NaOH溶液的反应不是皂化反应,故D错误;
故选B.
点评 本题考查有机物组成、结构与性质,题目难度不大,涉及苯的性质、有机反应类型、同分异构体等知识,明确常见有机物结构与性质即可解答,试题有利于提高学生的灵活应用能力.


科目:高中化学 来源:2017届贵州省高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列有关实验事实的解释中正确的是
选项 | 问题 | 解释 |
A | 实验室不能配制含有Fe3+、MnO4-、SO42-、Ba2+的中性溶液 | Fe3+水解呈酸性 |
B |
| 含有Ag+的溶液必然含有NO3-,在酸性条件下,可氧化Fe2+ |
C | 将氨气通入水中,形成的水溶液能导电 | 氨气是电解质 |
D | 在FeBr2溶液中通入过量Cl2,溶液变为棕黄色 | 发生反应2Fe2++Cl2===2Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 实验步骤 | 预期现象 | 结论 |
| 取少量A中残留物于试管中,加入适量稀硫酸,充分振荡使其完全溶解;将溶液分成两份,分别滴加高锰酸钾溶液、KSCN溶液 | 若高锰酸钾溶液不褪色,加入KSCN溶液后变红 | 固体残留物仅为Fe2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

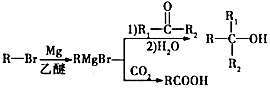
 ,其反应类型为取代反应.
,其反应类型为取代反应. .
. (写结构简式).
(写结构简式).
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com