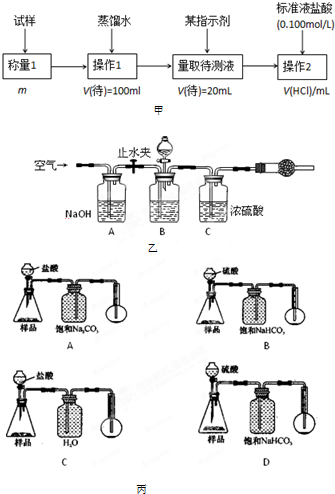
工业生产的纯碱中常含有少量NaCl杂质.为测定某纯碱样品的纯度,化学课外活动小组设计了三种实验方案:
方案一:取样品溶解后,加试剂使CO
32-沉淀,测定沉淀的质量.
方案二:用0.100mol/L盐酸滴定.
方案三用稀酸将CO
32-转化为CO
2,测定CO
2的质量.
(1)方案一的操作步骤有:①称量并溶解样品;②加入足量的BaCl
2溶液;③过滤;④洗涤;⑤干燥;⑥称量并进行恒重操作.称量时所需定量实验仪器为
电子天平
电子天平
.判断是否达到恒重的标准是
前后两次称量的质量差不超过0.001g
前后两次称量的质量差不超过0.001g
.
(2)方案二的具体过程如图甲:
①操作1所需要的仪器有
烧杯、玻璃棒、100mL容量瓶、胶头滴管
烧杯、玻璃棒、100mL容量瓶、胶头滴管
.
②滴定时选择的指示剂为甲基橙.当溶液
黄色恰好变成橙色,且半分钟内不褪色
黄色恰好变成橙色,且半分钟内不褪色
时,说明达到了滴定终点.
③为减少偶然误差,通常的处理办法是
做2-3次平行实验
做2-3次平行实验
.
④滴定时若锥形瓶内有少量液体溅出,则测定结果
偏低
偏低
.(选填“偏高”、“偏低”、“不影响”,下同),若盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗,测定结果
不影响
不影响
.
(3)方案三的实验装置如图乙:操作步骤有:①检查装置的气密性;②在干燥管内装满碱石灰,称量质量为W
1 g;③称量W
2 g样品装入广口瓶B中;④关闭止水夹;⑤缓慢加入稀H
2SO
4至不再产生气体为止;⑥打开止水夹;⑦缓缓鼓入空气数分钟,再称量干燥管,质量为W
3 g.该方案样品中纯碱的质量分数为
(用代数式表示).上图中装置A的作用是
吸收空气中的二氧化碳
吸收空气中的二氧化碳
.装置C的作用是
吸收二氧化碳中的水蒸气
吸收二氧化碳中的水蒸气
.有同学认为空气中的水蒸气会进入干燥管导致测量结果
偏大
偏大
(填“偏大”、“偏小”或“无影响”).改进措施可以是
在干燥管右边再加一个装有碱石灰的干燥管
在干燥管右边再加一个装有碱石灰的干燥管
.
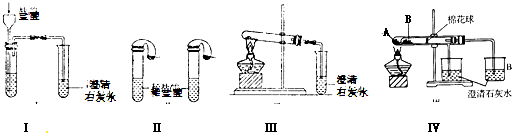
(4)若用如图丙装置对样品进行分析,根据量瓶中收集到的液体的体积来计算样品中碳酸钠的含量.则下列装置中,最合理的是
B
B
.(选填序号)


 工业生产的纯碱中常含有少量NaCl杂质.为测定某纯碱样品的纯度,化学课外活动小组设计了三种实验方案:
工业生产的纯碱中常含有少量NaCl杂质.为测定某纯碱样品的纯度,化学课外活动小组设计了三种实验方案: