
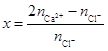 ��3�֣�����������Ҳ���֣�
��3�֣�����������Ҳ���֣�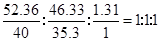
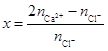



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��a��b��c��d | B��b��a��d��c | C��c��d��b��a | D��d��c��a��b |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.1mol | B��0.5mol | C��0.3 mol | D��0.7mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.045 mol��L | B��0.036 mol��L | C��0.026 mol��L | D��0.028 mol��L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��8.48�� | B��7.48�� | C��5.72�� | D��5.22�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��NH3 | B��HCl | C��SO2 | D��NO2�����費��N2O4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ijҺ���Ħ����������18g/mol��������ʵ��ܶ�һ����ˮ�� |
| B��ͬ��ͬѹ�£��ֱ���HCl��NO2����֧�Թܵ���������ˮ���㹻��ʱ�䣬���費�������ʵ���ɢ����֧�Թ�����Һ�����ʵ�����Ũ��֮��Ϊ3��2 |
| C����90%������Һ��10%������Һ�������ϣ�����������С��50% |
D��c mol/L��KCl��Һ���ܶ�Ϊd g/mL�����KCl��Һ����������Ϊ ��100% ��100% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
| �����ѧ��(CP)(500mL) Ʒ�������� ��ѧʽ��H2SO4 ��Է���������98 �ܶȣ�1.84g��cm-3 ����������98% |
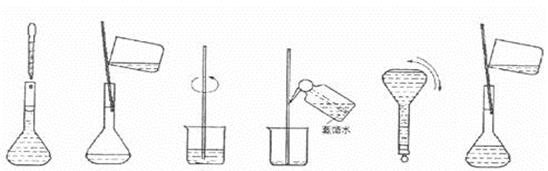
|
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com