
”¾ĢāÄæ”æij»ÆѧŠĖȤŠ”×é¶Ō2-äå±ūĶéÓėNaOHČÜŅŗ·¢ÉśµÄ·“Ó¦½ųŠŠĢ½¾æ£¬ŹµŃé×°ÖĆČēĻĀ£Ø¼Š³ÖŗĶ¼ÓČČ×°ÖĆŅŃĀŌČ„£©£ŗ

ŹµŃé²½Öč£ŗ
¢”£®½«Ō²µ×ÉÕĘæÓĆĖ®Ō”¼ÓČČ£¬ĄäÄż¹ÜÖŠĶØČėĄäÄżĖ®£»
¢¢£®½«·ÖŅŗĀ©¶·ÖŠµÄ2-äå±ūĶéÓėNaOHČÜŅŗµÄ»ģŗĻŅŗµĪČėŌ²µ×ÉÕĘæÄŚ”£
£Ø1£©Ė®ĄäÄż¹ÜaæŚŹĒ__________£ØĢī”°½ųĖ®æŚ”±»ņ”°³öĖ®æŚ”±£©”£
£Ø2£©Č”¾ßÖ§ŹŌ¹ÜÖŠŹÕ¼Æµ½µÄŅŗĢ壬¾ŗģĶā¹āĘ×¼ģ²ā£¬ĘäÖŠŅ»ÖÖĪļÖŹÖŠ“ęŌŚC-O¼üŗĶO-H¼ü”£ŌņøĆĪļÖŹµÄ½į¹¹¼ņŹ½ŹĒ_________________”£
£Ø3£©ŹµŃéÖŠĖįŠŌKMnO4ČÜŅŗĶŹÉ«£¬Éś³ÉøĆŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«µÄĪļÖŹµÄ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ____________________________________________________________”£
£Ø4£©ĶعżøĆŹµŃéµĆµ½µÄ½įĀŪŹĒ___________________________________________________”£
”¾“š°ø”æ ³öĖ®æŚ (CH3)2CHOH ![]() 2-äå±ūĶéÓėĒāŃõ»ÆÄĘČÜŅŗ¼ČÄÜ·¢ÉśČ”“ś·“Ó¦ÓÖÄÜ·¢ÉśĻūČ„·“Ó¦£¬Į½øö·“Ó¦ŌŚĶ¬Ņ»Ģõ¼žĻĀĶ¬Ź±·¢Éś
2-äå±ūĶéÓėĒāŃõ»ÆÄĘČÜŅŗ¼ČÄÜ·¢ÉśČ”“ś·“Ó¦ÓÖÄÜ·¢ÉśĻūČ„·“Ó¦£¬Į½øö·“Ó¦ŌŚĶ¬Ņ»Ģõ¼žĻĀĶ¬Ź±·¢Éś
”¾½āĪö”æ£Ø1£©ĪŖĮĖ³ä·ÖĄäČ“ÕōĘų£¬±ŲŠėŹ¹ĄäÄż¹ÜÄŚ³äĀśĄäČ“Ė®£¬¹ŹŠčŅŖµĶ½ųøß³ö£¬ĄäÄż¹ÜaæŚŹĒ³öĖ®æŚ£»(2) 2-äå±ūĶéÓėNaOHČÜŅŗ·“Ó¦µÄÉś³ÉĪļ½į¹¹ÖŠ“ęŌŚC-O¼üŗĶO-H¼ü£¬ŌņĖµĆ÷2-äå±ūĶéŌŚ“ĖĢõ¼ž·¢ÉśĮĖĖ®½ā·“Ӧɜ³ÉĮĖ(CH3)2CHOHŗĶäå»ÆÄĘ£»£Ø3£©»Ó·¢³öĄ“µÄŅŅ“¼¾Ė®Ļ“ŗóČܽāŌŚĖ®ÖŠ£¬2-äå±ūĶé·Šµć½Ļøß¾ĄäČ“ŗó²»»į½ųČėĖ®ÖŠ£¬ŅŖŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«£¬æÉÄÜŹĒŌŚĒ°Ćę·“Ó¦ÖŠ»¹Éś³ÉĮĖÄŃČÜÓŚĖ®ĒŅ·ŠµćµĶµÄĻ©Ģž£¬ĖłŅŌ·“Ó¦·½³ĢŹ½ĪŖ£ŗ![]() £»
£»
£Ø4£©ĶعżÉĻŹöŹµŃéĖµĆ÷2-äå±ūĶéÓėĒāŃõ»ÆÄĘČÜŅŗ¼ČÄÜ·¢ÉśČ”“ś·“Ó¦ÓÖÄÜ·¢ÉśĻūČ„·“Ó¦£¬Į½øö·“Ó¦ŌŚĶ¬Ņ»Ģõ¼žĻĀĶ¬Ź±·¢Éś”£


 ŠÄĖćæŚĖćĒÉĖćŅ»æĪŅ»Į·ĻµĮŠ“š°ø
ŠÄĖćæŚĖćĒÉĖćŅ»æĪŅ»Į·ĻµĮŠ“š°ø Ó¦ÓĆĢā×÷Ņµ±¾ĻµĮŠ“š°ø
Ó¦ÓĆĢā×÷Ņµ±¾ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷Ī¢Į£ÖŠ£¬ŗĖĶāµē×Ó×ÜŹżĻąµČµÄŹĒ£Ø £©
A.CO2 ŗĶ NO2
B.H2S ŗĶ H2O
C.NH4+ ŗĶ H2O
D.N2 ŗĶ C2H4
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČŪČŚÉÕ¼īѳʷӦŹ¹ÓĆĻĀĮŠĘ÷Ćó£Ø £©
A.ÉśĢśŪįŪö
B.ĘÕĶز£Į§ŪįŪö
C.ŹÆÓ¢ŪįŪö
D.“ÉŪįŪö
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķŹĒ¼øÖÖČõµē½āÖŹµÄµēĄėĘ½ŗā³£Źż (25”ę)”£
µē½āÖŹ | µēĄė·½³ĢŹ½ | Ę½ŗā³£ŹżK |
CH3COOH | CH3COOH | 1.76 ”Į 10 -5 |
H2CO3 | H2CO3 HCO3”Ŗ | K1=4.31 ”Į 10 -7 K2=5.61 ”Į 10 -11 |
C6H5OH | C6H5OH | 1.1 ”Į 10 -10 |
H3PO4 | H3PO4 H2PO4”Ŗ HPO42”Ŗ | K1=7.52 ”Į 10 -3 K2=6.23”Į 10 -8 K3=2.20”Į 10 -13 |
NH3”¤H2O | NH3”¤H2O | 1.76”Į 10 -5 |
»Ų“šĻĀĮŠĪŹĢā£ØC6H5OHĪŖ±½·Ó£©£ŗ
£Ø1£©ÓÉÉĻ±ķ·ÖĪö£¬Čō ¢Ł CH3COOH ¢Ś HCO3”Ŗ ¢Ū C6H5OH ¢Ü H2PO4”Ŗ ¾łæÉæ“×÷Ėį£¬ŌņĖüĆĒĖįŠŌÓÉĒæµ½ČõµÄĖ³ŠņĪŖ___________£ØĢī±ąŗÅ£©£»
£Ø2£©Š“³öC6H5OHÓėNa3PO4·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ__________________________£»
£Ø3£©25”ꏱ£¬½«µČĢå»żµČÅØ¶ČµÄ“×ĖįŗĶ°±Ė®»ģŗĻ£¬»ģŗĻŅŗÖŠ£ŗc(CH3COO”Ŗ)______c(NH4+)£»£ØĢī”°£¾”±”¢”°£½”±»ņ”°£¼”±£©
£Ø4£©25”ꏱ£¬Ļņ10 mL 0.01 mol/L±½·ÓČÜŅŗÖŠµĪ¼ÓV mL 0.01 mol/L°±Ė®£¬»ģŗĻČÜŅŗÖŠĮ£×ÓÅØ¶Č¹ŲĻµÕżČ·µÄŹĒ______£»
A.Čō»ģŗĻŅŗpH£¾7£¬ŌņV”Ż 10
B.Čō»ģŗĻŅŗpH£¼7£¬Ōņc((NH4+) £¾c (C6H5O”Ŗ) £¾c (H+)£¾c (OH”Ŗ)
C.V=10Ź±£¬»ģŗĻŅŗÖŠĖ®µÄµēĄė³Ģ¶ČŠ”ÓŚ10 mL 0.01mol/L±½·ÓČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č
D£®V=5Ź±£¬2c(NH3”¤H2O)+ 2 c (NH4+)= c (C6H5O”Ŗ)+ c (C6H5OH)
£Ø5£©Ė®½ā·“Ó¦ŹĒµäŠĶµÄæÉÄę·“Ó¦£®Ė®½ā·“Ó¦µÄ»ÆŃ§Ę½ŗā³£Źż³ĘĪŖĖ®½ā³£Źż(ÓĆKh±ķŹ¾)£¬Ąą±Č»ÆŃ§Ę½ŗā³£ŹżµÄ¶ØŅ壬ĒėŠ“³öNa2CO3µŚŅ»²½Ė®½ā·“Ó¦µÄĖ®½ā³£ŹżµÄ±ķ“ļŹ½_______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»ÆŗĻĪļXŹĒŅ»ÖÖĻć¶¹ĖŲŃÜÉśĪļ£¬æÉŅŌÓĆ×÷ĻćĮĻ£¬ĘäŗĻ³ÉĀ·ĻßČēĻĀ£ŗ

ŅŃÖŖ£ŗ
£Ø1£©AĖłŗ¬¹ŁÄÜĶŵÄĆū³ĘŹĒ___________”£
£Ø2£©BÉś³ÉC·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ___________________________________________”£
£Ø3£©GµÄ½į¹¹¼ņŹ½ŹĒ____________________”£
£Ø4£©FµÄ½į¹¹¼ņŹ½ŹĒ ”£DµÄ·Ö×ÓŹ½ŹĒC7H8O£¬ÓėF»„ĪŖĶ¬ĻµĪļ”£DµÄ½į¹¹¼ņŹ½ŹĒ________”£
”£DµÄ·Ö×ÓŹ½ŹĒC7H8O£¬ÓėF»„ĪŖĶ¬ĻµĪļ”£DµÄ½į¹¹¼ņŹ½ŹĒ________”£
£Ø5£©XµÄ·Ö×ÓŹ½ŹĒC13H14O2£¬XÓė×ćĮæNaOHČÜŅŗ¹²ČȵĻÆѧ·½³ĢŹ½ŹĒ________________”£
£Ø6£©EæÉŅŌ¾¶ą²½·“Ó¦ŗĻ³ÉF£¬ĒėŠ“³öŅ»ĢõæÉÄܵÄŗĻ³ÉĀ·ĻߣØÓĆ½į¹¹¼ņŹ½±ķŹ¾ÓŠ»śĪļ£¬ÓĆ¼żĶ·±ķŹ¾×Ŗ»Æ¹ŲĻµ£¬¼żĶ·ÉĻ×¢Ć÷ŹŌ¼ĮŗĶ·“Ó¦Ģõ¼ž£©__________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµŖŌŖĖŲæÉŅŌŠĪ³ÉŠķ¶ą»ÆŗĻĪļ£¬ŌŚĪŅĆĒÉś»īÉś²śÖŠÓŠ¹ć·ŗµÄÓ¦ÓĆ”£
(1) ÓėNF3·Ö×Ó»„ĪŖµČµē×ÓĢåµÄŅõĄė×ÓĪŖ________”£
(2) ĢśŗĶ°±ĘųŌŚ640 ”ęæÉ·¢ÉśÖĆ»»·“Ó¦£¬²śĪļÖ®Ņ»µÄ¾§°ū½į¹¹¼ūĶ¼”£Š“³öFe3£«µÄĶāĪ§µē×ÓÅŲ¼Ź½£ŗ_____________£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ_____________”£
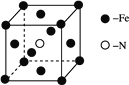
(3) Ī¬ÉśĖŲB4½į¹¹ČēĶ¼£¬Ōņ1 molĪ¬ÉśĖŲB4·Ö×ÓÖŠŗ¬ÓŠ¦Ņ¼üµÄŹżÄæĪŖ________mol”£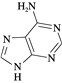
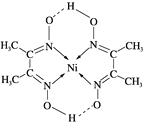
(4) ijÅäŗĻĪļµÄ½į¹¹ČēĶ¼£¬ĘäÖŠŗ¬ÓŠ________(ĢīŠņŗÅ)£»
a. ¼«ŠŌ¹²¼Ū¼ü””””””””””b. ·Ē¼«ŠŌ¹²¼Ū¼ü””””””””c. ÅäĪ»¼ü””””””””””d. Ēā¼ü
ĘäÖŠĢ¼Ō×ÓµÄŌӻƷ½Ź½ÓŠ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŌŗ¬īÜ·Ļ“߻ƼĮ(Ö÷ŅŖ³É·ÖĪŖCo”¢Fe”¢SiO2)ĪŖŌĮĻ£¬ÖĘČ”Ńõ»ÆīܵÄĮ÷³ĢČēĻĀ£ŗ
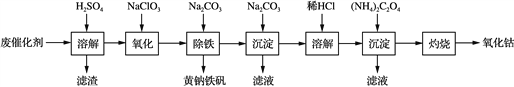
(1) Čܽā£ŗČܽāŗó¹żĀĖ£¬½«ĀĖŌüĻ“µÓ2”«3“Ī£¬ŌŁ½«Ļ“ŅŗÓėĀĖŅŗŗĻ²¢µÄÄæµÄŹĒ________________________________________________________________________”£
(2) Ńõ»Æ£ŗ¼ÓČČ½Į°čĢõ¼žĻĀ¼ÓČėNaClO3£¬½«Fe2£«Ńõ»Æ³ÉFe3£«£¬ĘäĄė×Ó·½³ĢŹ½ŹĒ____________________________”£
ŅŃÖŖ£ŗĢśĒč»Æ¼Ų»ÆѧŹ½ĪŖK3[Fe(CN)6]£»ŃĒĢśĒč»Æ¼Ų»ÆѧŹ½ĪŖK4[Fe(CN)6]”¤3H2O”£
3Fe2£«£«2[Fe(CN)6]3£===Fe3[Fe(CN)6]2”ż(Ą¶É«³Įµķ)
4Fe3£«£«3[Fe(CN)6]4£===Fe4[Fe(CN)6]3”ż(Ą¶É«³Įµķ)
Č·¶ØFe2£«ŹĒ·ńŃõ»ÆĶźČ«µÄ·½·ØŹĒ__________________________________”£(æɹ©Ń”ŌńµÄŹŌ¼Į£ŗĢśĒč»Æ¼ŲČÜŅŗ”¢ŃĒĢśĒč»Æ¼ŲČÜŅŗ”¢Ģś·Ū”¢KSCNČÜŅŗ)
(3) ³żĢś£ŗ¼ÓČėŹŹĮæµÄNa2CO3µ÷½ŚĖį¶Č£¬Éś³É»ĘÄĘĢś·Æ[Na2Fe6(SO4)4(OH)12]³Įµķ£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ_____________________________________________________”£
(4) ³Įµķ£ŗÉś³É³Įµķ¼īŹ½Ģ¼ĖįīÜ[(CoCO3)2”¤3Co(OH)2]£¬³ĮµķŠčĻ“µÓ£¬Ļ“µÓµÄ²Ł×÷ŹĒ________________________________________________________________________”£
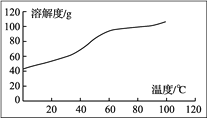
(5) Čܽā£ŗCoCl2µÄČܽā¶ČĒśĻßČēĶ¼ĖłŹ¾”£Ļņ¼īŹ½Ģ¼ĖįīÜÖŠ¼ÓČė×ćĮæĻ”ŃĪĖį£¬±ß¼ÓČČ±ß½Į°čÖĮĶźČ«Čܽāŗ󣬊č³ĆČČ¹żĀĖ£¬ĘäŌŅņŹĒ__________________________________________”£
(6) ×ĘÉÕ£ŗ×¼Č·³ĘČ”CoC2O4 1.470 g£¬ŌŚæÕĘųÖŠ³ä·Ö×ĘÉÕµĆ0.830 gŃõ»ÆīÜ£¬Š“³öŃõ»ÆīܵĻÆѧŹ½£ŗ________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖNaHSO4ŌŚĖ®ÖŠµÄµēĄė·½³ĢŹ½ĪŖ£ŗNaHSO4£½Na£«£«H£«£«SO42£”£Ä³ĪĀ¶ČĻĀ£¬ĻņpH£½6µÄÕōĮóĖ®ÖŠ¼ÓČėNaHSO4¾§Ģ壬±£³ÖĪĀ¶Č²»±ä£¬²āµĆČÜŅŗµÄpHĪŖ2”£ĻĀĮŠ¶ŌøĆČÜŅŗµÄŠšŹöÖŠ£¬²»ÕżČ·µÄŹĒ£Ø £©
A. øĆĪĀ¶ČøßÓŚ25”ę
B. ÓÉĖ®µēĄė³öĄ“µÄH£«µÄÅØ¶ČŹĒ1.0”Į10£10mol”¤L£1
C. NaHSO4¾§ĢåµÄ¼ÓČėŅÖÖĘĮĖĖ®µÄµēĄė
D. øĆĪĀ¶ČĻĀ¼ÓČėµČĢå»żpHĪŖ12µÄNaOHČÜŅŗæÉŹ¹øĆČÜŅŗĒ”ŗĆ³ŹÖŠŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĄ¬»ų¼Łµ„°ū¾śÖźÄܹ»ŌŚ·Ö½āÓŠ»śĪļµÄĶ¬Ź±·ÖĆŚĪļÖŹ²śÉśµēÄÜ£¬ĘäŌĄķČēĻĀĶ¼ĖłŹ¾”£ÓŠ»śĪļĪŖC6H12O6)”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A. AĪŖÕż¼«£¬H2PCAŌŚøƵē¼«ÉĻ·¢ÉśŃõ»Æ·“Ó¦
B. ·Åµē¹ż³ĢÖŠ£¬Õż¼«·“Ó¦ĪŖ2H2O-4e=4H++O2”ü
C. Čō1molO2²ĪÓėµē¼«·“Ó¦£¬ÓŠ2 mol H+“©¹żÖŹ×Ó½»»»Ä¤½ųČėÓŅŹŅ
D. µē³Ų×Ü·“Ó¦ĪŖ:C6H12O6+6O2![]() 6CO2”ü+6H2O
6CO2ӟ+6H2O
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com