
 ������Ԫ��E��R��X��Y��Z��ԭ��������������������ɵĵ��ʻ��������ͼת����ϵ���ס���Ϊ��Ԫ���������Ϊ���ʣ�������Ϊ��Ԫ������.25��ʱ��0.1 mol•L-1����Һ��pH=1��0.1mol•L-1����Һ��pH=13����������Һ���ʱ������ɫ�����������ƶϲ���ȷ���ǣ�������
������Ԫ��E��R��X��Y��Z��ԭ��������������������ɵĵ��ʻ��������ͼת����ϵ���ס���Ϊ��Ԫ���������Ϊ���ʣ�������Ϊ��Ԫ������.25��ʱ��0.1 mol•L-1����Һ��pH=1��0.1mol•L-1����Һ��pH=13����������Һ���ʱ������ɫ�����������ƶϲ���ȷ���ǣ�������| A�� | �����Ӱ뾶��r��Z����r��R����r��X����r��Y�� | |
| B�� | X��Y��Z������������Ӧ��ˮ�������Ӧ | |
| C�� | R��E��Z�ɴ�����ͬһ�ֹ��ۻ������� | |
| D�� | Z�������Ӷ�����������R��������ǿ |
���� 25��ʱ��0.1 mol•L-1����Һ��pH=1��˵����ΪһԪǿ�ᣬ��Ϊ��Ԫ�������������ֻ��HCl���㣻0.1mol•L-1����Һ��pH=13��˵����ΪһԪǿ�������Ԫ����ֻ��Na��Ӧ��NaOHΪǿ�����EΪHԪ�أ���Ϊ���ʣ��ܹ���ǿ��ס�ǿ�����Ӧ���ɵ����죬����ֻ��Ϊ��������Ϊ����Al�����E��R��X��Y��Z��ԭ���������������֪EΪH��O��Na��Al��ClԪ�أ��ݴ˽��Ԫ��������֪ʶ���
��� �⣺25��ʱ��0.1 mol•L-1����Һ��pH=1��˵����ΪһԪǿ�ᣬ��Ϊ��Ԫ�������������ֻ��HCl���㣻0.1mol•L-1����Һ��pH=13��˵����ΪһԪǿ�������Ԫ����ֻ��Na��Ӧ��NaOHΪǿ�����EΪHԪ�أ���Ϊ���ʣ��ܹ���ǿ��ס�ǿ�����Ӧ���ɵ����죬����ֻ��Ϊ��������Ϊ����Al�����E��R��X��Y��Z��ԭ���������������֪EΪH��O��Na��Al��ClԪ�أ�
A�����ӵĵ��Ӳ�Խ�࣬���Ӱ뾶Խ���Ӳ���ͬʱ�����ӵĺ˵����Խ�����Ӱ뾶ԽС���������Ӱ뾶��СΪ��r��Z����r��R����r��X����r��Y������A��ȷ��
B��X��Y��Z������������Ӧ��ˮ����ֱ�ΪNaOH��Al��OH��3��HClO4����������Ϊ�������������������֮�������Ӧ����B��ȷ��
C��R��E��Z�ֱ�ΪO��H��ClԪ�أ����ֿ����γɹ��ۻ���������ᡢ�����ᣬ��C��ȷ��
D��Z��������Ϊ�����ӣ�R��������Ϊ�����ӣ���Ӧ�⻯��Խ�ѵ��룬�����������Խǿ������HClΪǿ����ʣ�ˮΪ������ʣ��������ӽ����������С�������ӣ���Z�������Ӷ�����������R��������������D����
��ѡD��
���� ���⿼��Ԫ���ƶϡ�ԭ�ӽṹ��Ԫ�������ɵ�Ӧ�ã���Ŀ�Ѷ��еȣ���ȷ�ƶ�Ԫ��Ϊ���ؼ���ע����������ԭ�ӽṹ��Ԫ�������ɡ�Ԫ�����ڱ��Ĺ�ϵ���������������ѧ���ķ���������������������


 ������ҵ����ν�����������ϵ�д�
������ҵ����ν�����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 һ���¶��£���һ������A��B��������ܱ�������������Ӧ��A��g��+B��g��?xC��g��+3D����������Ӧƽ��ı�Ӱ��ƽ���һ������������A��Ũ�ȱ仯��ͼ��ʾ�������й�˵����ȷ���ǣ�������
һ���¶��£���һ������A��B��������ܱ�������������Ӧ��A��g��+B��g��?xC��g��+3D����������Ӧƽ��ı�Ӱ��ƽ���һ������������A��Ũ�ȱ仯��ͼ��ʾ�������й�˵����ȷ���ǣ�������| A�� | x=2��CΪ��̬��D����Ϊ��̬Ҳ����Ϊ����̬ | |
| B�� | �ı������������ʹ���˴��� | |
| C�� | �����������䣬�����������ټ�������C��ƽ�������ƶ���ƽ�ⳣ������ | |
| D�� | �÷�Ӧ�Ļ�ѧƽ�ⳣ��K=$\frac{{c}^{2}��C��}{[c��A��•c��B��]}$�����¶����ߣ�Kֵ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1Lˮ�к���1mol NaCl | |
| B�� | ��Һ�к���1mol NaCl | |
| C�� | 1L��Һ�к���58.5g NaCl | |
| D�� | ��58.5g NaCl����1Lˮ�����õ���Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���������ࡱ��ʵ���������30%�Ĺ���������Һ�м��������������̺ͱ�����Լ���������ͼ��
���������ࡱ��ʵ���������30%�Ĺ���������Һ�м��������������̺ͱ�����Լ���������ͼ��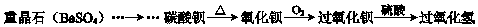
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������Ӧ�ġ�H��� | B�� | �����¶ȣ����������ܶ����� | ||
| C�� | ѹ����������Ӧ���յ��������� | D�� | ���������MgO��������CO��ת���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 50mL | B�� | 60mL | C�� | 70mL | D�� | 80mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com