
| A、一种纯净的化合物 |
| B、一种单质和一种化合物的混合物 |
| C、两种化合物的混合物 |
| D、两种单质的混合物 |


科目:高中化学 来源: 题型:
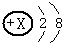 请回答:
请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、12g石墨烯(单层石墨)中含有六元环的个数为0.5N0 |
| B、1.0L1.0mo1?L-1的NaNO3水溶液中含有的氧原子数为3N0 |
| C、25℃时pH=13的NaOH溶液中含有OH一的数目为0.1 N0 |
| D、1 mol的羟基与1 mol的氢氧根离子所含电子数均为9 N0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钡溶液与稀硫酸的反应OH-+H+=H2O |
| B、氧化镁与稀盐酸反应MgO+2H+=Mg2++H2O |
| C、铜片插入硝酸银溶液中Cu+Ag+=Cu2++Ag |
| D、少量碳酸钙溶于稀盐酸中CaCO3+2H+=Ca2++H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、三者对应的氧化物均为酸性氧化物 |
| B、实验室可用NaOH溶液处理SO2、NO2 |
| C、CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
| D、三者的单质直接与氧气反应都能生成两种氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
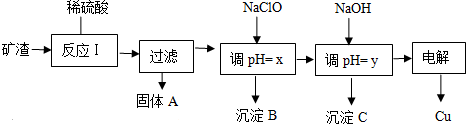
查看答案和解析>>
科目:高中化学 来源: 题型:
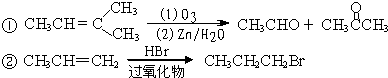
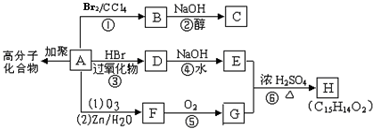
查看答案和解析>>
科目:高中化学 来源: 题型:
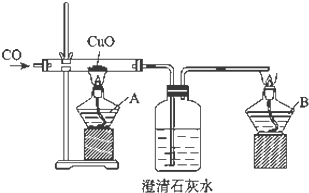 证明CO具有还原性的实验装置,如图所示.
证明CO具有还原性的实验装置,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
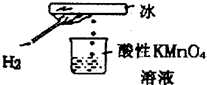 某化学研究性学习小组在老师指导下做了一个如图所示的实验,发现烧杯中酸性KMnO4溶液褪色.若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,溶液显红色.判断下列说法中正确的是( )
某化学研究性学习小组在老师指导下做了一个如图所示的实验,发现烧杯中酸性KMnO4溶液褪色.若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,溶液显红色.判断下列说法中正确的是( )| A、该条件下生成的水分子化学性质比较活泼 |
| B、该条件下H2被冷却为液态氢,液氢的水溶液具有还原性 |
| C、该条件下H2燃烧生成了具有还原性的物质 |
| D、该条件下H2燃烧的产物中可能含有一定量的H2O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com