
| A. | Fe3+、K+、Ag+、NO3-、 | B. | Na+、K+、CO32-、C1- | ||
| C. | NH4+、Al3+、Cl-、NO3- | D. | Mg2+、Na+、CO32-、SO42- |
 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:选择题
| A. | 将Fe2O3粉碎 | B. | 保持容器体积不变,增加H2输入量 | ||
| C. | 充入N2,保持容器内压强不变 | D. | 充入N2,保持容器内体积不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
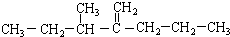 此烃名称为3-甲基-2-丙基-1-戊烯.
此烃名称为3-甲基-2-丙基-1-戊烯.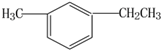 的烃可命名为-甲基-3-乙基苯.
的烃可命名为-甲基-3-乙基苯.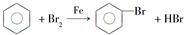 ,此反应属于取代反应.
,此反应属于取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标况下,22.4L氯气完全溶于水转移电子数为NA | |
| B. | 32gS完全溶于氢氧化钠溶液转移电子数为2 NA | |
| C. | 标况下,6.72LNO2完全溶于水转移电子数为NA | |
| D. | 28.8g氧化亚铜溶于稀硫酸转移电子数为0.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 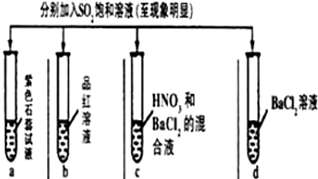 | ||||
| 记录 | A | 无色 | 无色 | 无色溶液 | 无色溶液 |
| B | 红色 | 无色 | 白色沉淀 | 白色沉淀 | |
| C | 红色 | 无色 | 白色沉淀 | 无色溶液 | |
| D | 无色 | 无色 | 无色溶液 | 无色溶液 | |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.0mol/L | B. | 1.5 mol/L | C. | 0.18 mol/L | D. | 0.24mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
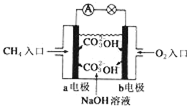 人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.
人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com