
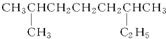 系统命名:2,6二甲基辛烷;
系统命名:2,6二甲基辛烷; ;
; ;②乙醛与银氨溶液水浴加热CH3CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3COONH4+2Ag+3NH3+H2O;
;②乙醛与银氨溶液水浴加热CH3CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3COONH4+2Ag+3NH3+H2O;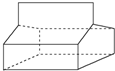
分析 (1)烷烃命名时,要选择最长的碳链为主链,从离支链近的一端给主链上碳原子进行编号;
(2)烷烃中含有取代基乙基,则主链至少含有5个C原子,据此写出满足条件的烷烃的结构简式;
(3)有机化合物中具有同一通式、组成上相差一个或多个某种原子团、在结构与性质上相似的化合物系列,为同系物;具有相同分子式而结构不同的化合物互为同分异构体;
(4)①丙烯发生加聚反应生成聚丙烯;②乙醛和银氨溶液水浴加热发生银镜反应生成氨气、银、醋酸铵和水;
(5)①交点为C原子,交点之间的短线是化学键,利用H原子饱和碳的四价结构,据此书写分子式;
②根据篮烷的结构可知,其属于环烷烃,故不溶于水,且由于其相对分子质量比较大,故熔沸点比较高,不是气体,据此分析其性质;
③篮烷的氢原子有几种,其一氯代物就有几种,据此分析.
解答 解:(1)烷烃命名时,要选择最长的碳链为主链,则主链上有8个碳原子,从离支链近的一端给主链上碳原子进行编号,则在2号和6号碳原子上各有一个甲基,故名称为:2,6二甲基辛烷,故答案为:2,6二甲基辛烷;
(2)采用知识迁移的方法解答,该烷烃相当于甲烷中的氢原子被烃基取代,如果有乙基,主链上碳原子最少有5个,所以该烃相当于甲烷中的3个氢原子被乙基取代,故该烃的结构简式 ,故答案为
,故答案为 ;
;
(3)2-甲基戊酸与丁酸组成上相差1个CH2原子团,二者互为同系物;新戊烷与2,3-二甲基丙烷是同一种物质;对羟基苯甲醛与甲酸苯酚酯、丙烯醇与丙酮分子式相同,结构不同,互为同分异构体,故答案为:C;A;B;B;
(4)①丙烯发生加聚反应生成聚丙烯,化学方程式为 ,故答案为:
,故答案为: ;
;
②乙醛和银氨溶液水浴加热发生银镜反应生成氨气、银、醋酸铵和水,化学方程式:CH3CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3COONH4+2Ag+3NH3+H2O,
故答案为:CH3CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3COONH4+2Ag+3NH3+H2O;
(5)①由蓝烷的结构可知,分子中含有12个C原子、14个H原子,分子式为C12H14,故答案为:C12H14;
②根据篮烷的结构可知,其属于环烷烃.
a、烃类均不溶于水,故a不选;
b、烃类的密度均比水小,故b选;
c、由于篮烷属于环烷烃,故不能和溴水发生加成发生,故c选;
d、由于其相对分子质量比较大,故熔沸点比较高,在常温下不是气体,故d选.
故选bcd;
④该分子属于高度对称结构,有如图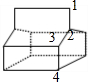 所示的4种H原子,故其一氯代物就有几种同分异构体,故答案为:4.
所示的4种H原子,故其一氯代物就有几种同分异构体,故答案为:4.
点评 本题考查有机物的结构、五同的区别,化学方程式的书写、同分异构体等,难度中等,实际是键线式结构,注意对结构的仔细观察.


科目:高中化学 来源: 题型:选择题
| A. | 无色溶液中:Cr2O${\;}_{7}^{2-}$、Fe3+、SCN-、Cl- | |
| B. | 能使石蕊呈蓝色的溶液中:Na+、K+、NO${\;}_{3}^{-}$、CO${\;}_{3}^{2-}$ | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012 的溶液中:S2O${\;}_{3}^{2-}$、CrO${\;}_{4}^{2-}$、Cl-、Mg2+ | |
| D. | 水电离的c (H)=10-12mol•L-1 的溶液中:HCO${\;}_{3}^{-}$、SiO${\;}_{3}^{2-}$、Cu2+、NH${\;}_{4}^{+}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由于电流的作用,酸、碱、盐溶于水发生电离 | |
| B. | 胶体的分散质粒子直径小于l00nm但大于1nm,能通过滤纸,不能透过半透膜 | |
| C. | 存在自由移动的离子是电解质溶液导电的原因 | |
| D. | 向氢氧化铁胶体中滴加稀硫酸,开始时产生沉淀,继续滴加时沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
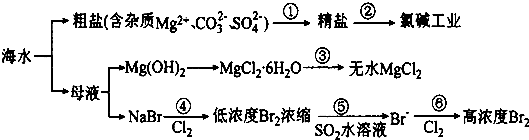
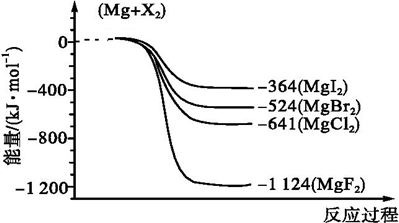
| A. | 过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 | |
| B. | 过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 | |
| C. | 在过程④、⑥反应中每氧化0.2 mol Br一需消耗2.24LCl2 | |
| D. | 在过程③中将MgCl2.6H2O灼烧即可制得无水MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图所示的装置常用于制取气体并检验气体的性质.下列有关说法正确的是( )
如图所示的装置常用于制取气体并检验气体的性质.下列有关说法正确的是( )| A. | 关闭分液漏斗的活塞.将干燥管末端放人水中,微热烧瓶,有气泡从水中冒出,停止加热后,燥管内有水柱形成,表明装置不漏气 | |
| B. | 若装置用于制取氯气并验证其具有漂白性,则A中所用试剂为稀盐酸,B中所用药品为KMnO4固体,C中为品红溶液 | |
| C. | 若装置用于制取SO2并验证其具有漂白性,则A中所用试剂为浓硫酸,B中所用药品为Na2SO3固体,C中为酸性KMnO4溶液 | |
| D. | 若实验时B中盛放固体NaOH,A中为浓氨水,C中为稀AgNO3溶液,则实验过程中,C试管中看不到明显的实验现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Na+)>c(HCO${\;}_{3}^{-}$)>c(H+)>c(OH-) | |
| B. | c(HCO${\;}_{3}^{-}$)>c(ClO-)>c(OH-) | |
| C. | c(HClO)+c(ClO-)=c(HCO${\;}_{3}^{-}$)+c(H2CO3) | |
| D. | c(Na+)+c(H+)=c(HCO${\;}_{3}^{-}$)+c(ClO-)+c(OH-)+c(CO${\;}_{3}^{2-}$) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com