
分析 (1)丙醛与银氨溶液在水浴加热条件下反应生成丙酸铵、水、银、氨气;
(2)丙醛与新制的氢氧化铜悬浊液在加热条件下发生反应生成丙酸和氧化亚铜;
(3)丙醛与氢气在催化剂条件下发生加成反应生成1-丙醇;
解答 解:(1)丙醛与银氨溶液在水浴加热条件下反应生成丙酸铵、水、银、氨气,方程式:CH3CH2CHO+2Ag(NH3)2OH $\stackrel{△}{→}$CH3CH2COONH4+2Ag+3NH3+H2O,
故答案为:CH3CH2CHO+2Ag(NH3)2OH $\stackrel{△}{→}$CH3CH2COONH4+2Ag+3NH3+H2O;
(2)丙醛与新制的氢氧化铜悬浊液在加热条件下发生反应生成丙酸和氧化亚铜,方程式为:CH3CH2CHO+2Cu(OH)2$\stackrel{△}{→}$CH3CH2COOH+Cu2O↓+2H2O,
故答案为:CH3CH2CHO+2Cu(OH)2$\stackrel{△}{→}$CH3CH2COOH+Cu2O↓+2H2O;
(3)丙醛与氢气在催化剂条件下发生加成反应生成1-丙醇,方程式:CH3CH2CHO+H2$\stackrel{催化剂}{→}$CH3CH2CH2OH,
故答案为:CH3CH2CHO+H2$\stackrel{催化剂}{→}$CH3CH2CH2OH.
点评 本题考查了化学方程式的书写,侧重考查有机反应方程式书写,熟悉有机物结构特点及性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
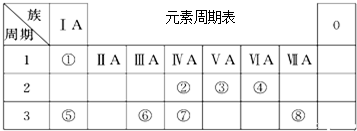
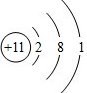 .?③元素形成的单质的电子式为:
.?③元素形成的单质的电子式为: .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点:NH3>PH3>AsH3 | B. | 熔点:SiO2>NaCl>CH4 | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol溴苯中含有双键的数目为0.3NA | |
| B. | 1L 0.1 mol/L醋酸溶液中含有醋酸分子的数目为0.1 NA | |
| C. | 常温下,1 L pH=1的H2SO4溶液中,由水电离出的H+数目为0.1NA | |
| D. | 常温下,9.2gNO2和N2O4的混合气体中含有的氮原子数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z为0.3 mol•L-1 | B. | Y2为0.1 mol•L-1 | C. | X2为0.2 mol•L-1 | D. | Z为0.4 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
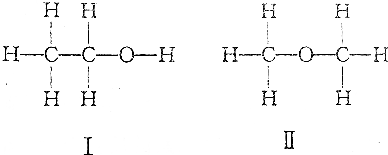
| A. | Ⅰ和Ⅱ是同分异构体 | B. | Ⅰ和Ⅱ物理性质有所不同 | ||
| C. | Ⅰ和Ⅱ化学性质相同 | D. | Ⅰ和Ⅱ含12C的质量分数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
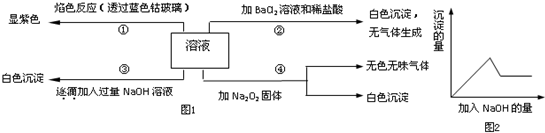
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
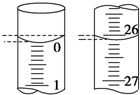 氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之).现用0.1000mol•L-1KMnO4酸性溶液滴定未知浓度的无色H2C2O4溶液,反应离子方程式是:2MnO${\;}_{4}^{-}$+5H2C2O4+6H+═2Mn2++CO2↑+8H2O.
氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之).现用0.1000mol•L-1KMnO4酸性溶液滴定未知浓度的无色H2C2O4溶液,反应离子方程式是:2MnO${\;}_{4}^{-}$+5H2C2O4+6H+═2Mn2++CO2↑+8H2O.| 滴定次数 | 待测H2C2O4溶液的体积/mL | 0.1000 mol•L-1 KMnO4的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 2 8.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
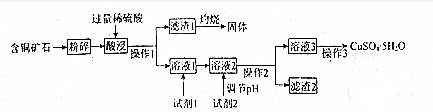
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Cu(OH)2 | 4.0 | 6.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com