
��10�֣���2molSO2��1molO2�����������ɱ䣬ѹǿ�㶨���ܱ������У���һ���¶��·������·�Ӧ��2SO2(g)+O2(g)  2SO3(g)����H��0������Ӧ���е�ʱ��t1��ʱ�ﵽƽ��״̬����û�����������ʵ���Ϊ2.1 mol���Իش��������⣺
2SO3(g)����H��0������Ӧ���е�ʱ��t1��ʱ�ﵽƽ��״̬����û�����������ʵ���Ϊ2.1 mol���Իش��������⣺
��1����Ӧ���е�t1ʱ��SO2���������Ϊ ��
��2������t1ʱ����һ�����������Ar��,SO2�����ʵ����� �����������С�����䡱����
��3������t1ʱ���£����´ﵽƽ��״̬����ƽ������������������ʵ��� 2.1mol���<������>����=��������˵��ԭ�� ��
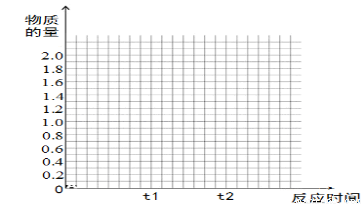
��4���������������䣬��t1ʱ�ټ���0.2molSO2��0.1molO2 ��1.8molSO3����ͼ��������t0��t1��t2�����ʱ����SO2�����ʵ����仯���ߡ�
 ���100��1�ž�ϵ�д�
���100��1�ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�갲��ʡ��һ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����Ϊ100mL��Ũ�Ⱦ�Ϊ1mol��L-1�������������Һ���ֱ����������ȵ�þ���ַ�Ӧ�������ɵ���������ͬ�����������Ϊ2��3����þ�������Ϊ
A��1.8 g B��2.4g C��3.6g D��4.8g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣��ʡ�߶���ѧ�ڰ��ڿ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
n L������̬�������������������ϵ�ȼ�ָ���ԭ��״̬�����³�ѹ�����������С2n L���������������ܵ������
A��CH4��C2H4��C3H4������Ȼ��
B��C2H6��C4H6��C2H2��2:1:2�����ʵ���֮�Ȼ��
C��C3H8��C4H8��C2H2��11:14:26������֮�Ȼ��
D��CH4��C3H6��C2H2��a:b:b����Ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭�յ�����ѧ�߶���10���¿���ѧ�Ծ��������棩 ���ͣ������
��10�֣��������и������

��1���������黯��������ͬϵ����� ������ͬ���칹����� �������ţ���
��2��A��B��C�еĻ������к��еĹ������ǣ�д���ƣ� �� �� �� ��
��3�����ݹ����ŵ��ص�ɽ�C���������ﻮ��Ϊ ��� �ࡣ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�갲��ʦ������ѧ�߶������в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�л����������̼���⡢������Ԫ����ɣ�����Է�������С��150������֪����������������Ϊ50%�����������ԭ�ӵĸ���������
A��1��4 B��2��3 C��ֻ��4 D��1��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ��һ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ҵ�ϳ���FeCl3��Һ��ͭ��Ӧ����ӡˢ��·�塣�÷�Ӧ�Ļ�ѧ����ʽΪ��2FeCl3+Cu =2FeCl2+CuCl2��ȡ������Ӧ����Һ10 mL���з������������c(Fe3+)Ϊ1mol��L��1�������м�����������������Һ�����ˡ�����ɵõ�����l7.22g����������Ӧ���10mL��Һ��c(Cu2+)Ϊ
A��0.5mol��L��1 B��1.5 mol��L��1 C��0.4 mol��L��1 D��0.25 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶��ϵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���ܱ������н������·�Ӧ��X2������ + Y2������  2Z�������� ��֪ X2��Y2��Z����ʼŨ�ȷֱ�Ϊ 0.1 mol/L��0.3 mol/L��0.2 mol/L�� ��һ���������£� ����Ӧ�ﵽƽ��ʱ�������ʵ�Ũ���п�����
2Z�������� ��֪ X2��Y2��Z����ʼŨ�ȷֱ�Ϊ 0.1 mol/L��0.3 mol/L��0.2 mol/L�� ��һ���������£� ����Ӧ�ﵽƽ��ʱ�������ʵ�Ũ���п�����
A��Y2Ϊ0.2 mol/L B��Y2 Ϊ0.35 mol/L
C��X2 Ϊ0.2 mol/L D�� ZΪ 0.4 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������������ѧ������ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ������
��14�֣����Ǻϳ����ᡢ��κ͵��ʵĻ���ԭ�ϣ����ʣ�
��1������ˮ��Һ�������ԣ���ԭ��Ϊ �������ӷ���ʽ��ʾ����0.1 mol•L-1�İ�ˮ�м���������NH4Cl���壬��Һ��PH ������ߡ����͡�������������������������Һ�е�NH4+��Ũ�� �������С������
��2������識��ȷֽ�ɵõ�N2O��H2O��250��ʱ����������ܱ������зֽ�ﵽƽ�⣬�÷ֽⷴӦ�Ļ�ѧ����ʽΪ ��ƽ�ⳣ������ʽΪ ������1mol�������ȫ�ֽ⣬ת�Ƶĵ�����Ϊ mol��
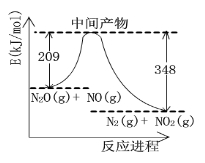
��3����N2O��NO��Ӧ����N2��NO2�������仯��ͼ��ʾ�� ������1mol N2�����H= kJ•mol-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������ѧ��10��������ѧ�Ծ��������棩 ���ͣ�ʵ����
��10�֣����������Һ���������ʵĶ��Լ����붨��������
��1��ʵ����������KMnO4����������250.00 mL 0.1000 mol•L-1��KMnO4������Һ��
�����õ���������ƽ��ҩ�ס��ձ�������������Ͳ�� �� ��
�����ƹ����в���������������� ��
�����в�����ʵ������Ӱ��ƫ����� ������ţ���
a����ˮ����ʱ���ӿ̶���
b������ƿ�ڱڸ���ˮ���δ���ﴦ��
c���ߵ�ҡ�Ⱥ��ְ�Һ����ڿ̶����ּ�ˮ����
��2������������KMnO4��Һ���ⶨFeSO4��Һ��Fe2+�����ʵ���Ũ�ȡ�
����ƽ�÷�Ӧ�Ļ�ѧ����ʽ��FeSO4 + KMnO4 + H2SO4  K2SO4 + MnSO4 + Fe2(SO4)3 + H2O
K2SO4 + MnSO4 + Fe2(SO4)3 + H2O
��ʵ��ʱӦ�ⶨ�������У���ȡFeSO4��Һ������� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com