
| A. | 铝的第一电离能比镁的第一电离能大 | |
| B. | 钾的第一电离能比镁的第一电离能大 | |
| C. | 在所有的元素中,F的第一电离能最大 | |
| D. | 第3周期所含元素中钠的第一电离能最小 |
分析 A.镁原子的3s能级处于全满稳定状态,能量较低,第一电离能比Al元素高;
B.同主族自上而下第一电离能降低,同周期自左而右第一电离能增大;
C.同周期主族元素从左到右作用到电离能逐渐增大,到稀有气体由于具有稳定的电子层结构,其电离能最大;
D.同周期自左而右,元素的第一电离能增大,注意能级处于半满、全满的稳定特殊情况.
解答 解:A.镁原子的3s能级处于全满稳定状态,能量较低,第一电离能比Al元素高,故A错误;
B.同主族自上而下第一电离能降低,故第一电离能Na>K,同周期自左而右第一电离能增大,故第一电离能Mg>Na,所以第一电离能Mg>K,故B错误;
C.同周期主族元素从左到右作用到电离能逐渐增大,同族元素从上到下第一电离能逐渐减小,则氦的第一电离能最大,故C错误;
D.同周期自左而右,元素的第一电离能增大,故第3周期所包含的元素中钠的第一电离能最小,故D正确;
故选D.
点评 本题考查第一电离能的变化规律等,比较基础,注意同周期主族元素能级处于半满、全满的稳定特殊情况第一电离能增大的特殊情况,题目难度不大.


 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 化学反应的实质是旧化学键断裂和新化学键的形成 | |
| B. | 物质由高能量向低能量转化时,放出热量 | |
| C. | 将一定质量的C燃烧,生成CO2时比生成CO时放出的热量多 | |
| D. | 干冰升华时放出大量的热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 装置 | 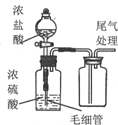 | 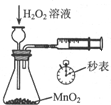 | 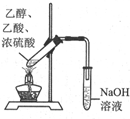 | 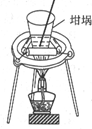 |
| 目的 | 快速制取少量HCl气体 | 测定不同浓度的H2O2溶液对产生O2速率的影响 | 制备并收集乙酸乙酯 | 从小苏打溶液中提取NaHCO3晶体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
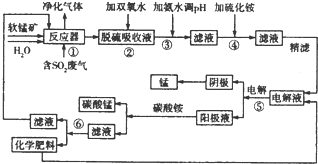
| 阳离子 | Fe2+ | Fe3+ | Mn2+ | Ni2+ | Co2+ | |
| 氢氧化物沉淀 | 开始沉淀的PH | 7.5 | 2.2 | 8.8 | 6.4 | 9.0 |
| 完全沉淀的PH | 9.5 | 3.5 | 10.8 | 8.4 | ||
| 硫化物沉淀 | 开始沉淀的PH | 6.2 | 4.67 | |||
| 完全沉淀的PH | ||||||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某同学按如图所示的装置进行实验.A、B为两种常见金属,它们的硫酸盐可溶于水.当K闭合时,在交換膜处
某同学按如图所示的装置进行实验.A、B为两种常见金属,它们的硫酸盐可溶于水.当K闭合时,在交換膜处| A. | 反应初期,x电极周围出现白色胶状沉淀,不久沉淀溶解 | |
| B. | 溶液中(A2+)减小 | |
| C. | y电极上有H2产生,发生还原反应 | |
| D. | B的电极反应:B-2e═B2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | P、Q、R、S的浓度相等 | B. | P、Q、R、S在容器中共存 | ||
| C. | P、Q的反应速率相等内部 | D. | P、Q、R、S的浓度不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石与碳纳米管互为同素异形体 | B. | N5与N2互为同素异形体 | ||
| C. | 14C的质子数为14 | D. | 乙醇和二甲醚属于同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
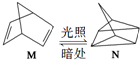 △H=+88.6kJ•mol-1
△H=+88.6kJ•mol-1查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子数和质量分别不等 | B. | 质子数相等,质量不等 | ||
| C. | 分子数和质量都相等 | D. | 原子数、中子数和质子数都相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com