
分析 (1)运用盖斯定律解答,注意分析待求反应中的反应物和生成物在已知反应中的位置,通过加减求得;
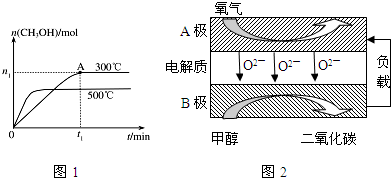
(2)在300℃到500℃时,物质的量n(CH3OH)减小,平衡逆向移动;
(3)改变条件平衡正向移动,由此分析;
(4)依据化学平衡三段式列式计算平衡浓度,结合平衡常数概念计算得到;
(5)①根据原电池原理,负极上甲醇失电子生成二氧化碳;
②根据电池中的能量转化率分析;
(6)根据c(Ca2+)•c (C2O42-)和Ksp(4.0×10-8)相对大小判断,如果c(Ca2+)•c (C2O42-)=<Ksp(4.0×10-8),则无沉淀生成.
解答 解:(1)①CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H1
②2CO(g)+O2(g)=2CO2(g)△H2
③2H2(g)+O2(g)=2H2O(g)△H3
据盖斯定律,①+$\frac{1}{2}$②-$\frac{1}{2}$③得:CO(g)+2H2(g)?CH3OH(g)△H=△H1+$\frac{1}{2}$△H2-$\frac{1}{2}$△H3,
故答案为=△H1+$\frac{1}{2}$△H2-$\frac{1}{2}$△H3;
(2)在300℃到500℃时,物质的量n(CH3OH)减小,平衡逆向移动,逆反应是吸热反应,正反应是放热反应,故答案为:<;
(3)A.缩小容器体积,增大压强,平衡正向移动,甲醇的产率增加,故正确;
B.降低温度,平衡正向移动,甲醇的产率增加,故正确;
C.升高温度,平衡逆向移动,甲醇的产率减少,故错误;
D.使用合适的催化剂,平衡不移动,故错误;
E.将甲醇从混合体系中分离出来,有利平衡正向移动,提高甲醇的产量,故正确;
故选:ABE;
(4)CH4和H2O在催化剂表面发生反应CH4+H2O?CO+3H2,T℃时,向1L密闭容器中投入1mol CH4和1mol H2O(g),5小时后测得反应体系达到平衡状态,此时CH4的转化率为50%,
CH4 +H2O?CO+3H2
起始物质的量浓度(mol•L-1) 1.0 1.0 0 0
转化物质的量浓度(mol•L-1) 0.5 0.5 0.5 1.5
平衡物质的量浓度(mol•L-1 0.5 0.5 0.5 1.5
K=$\frac{{c}^{3}({H}_{2})•c(CO)}{c(C{H}_{4})•c({H}_{2}O)}$=$\frac{0.5×1.{5}^{3}}{0.5×0.5}$=6.75mol2/L2;
故答案为:6.75;
(5)①根据原电池原理,负极上甲醇失电子生成二氧化碳,电极反应为:CH3OH+3O2--6e-=CO2+2H2O,故答案为:CH3OH+3O2--6e-=CO2+2H2O;
②甲醇不完全被氧化,生成C或CO或者原电池中发生反应时化学能不去全部转化为电能,即电池能量转化率达不到100%,所以实际上消耗的甲醇的质量比理论上大,
故答案为:甲醇不完全被氧化,生成C或CO 或电池能量转化率达不到100%;
(6)碳酸钙溶液中钙离子浓度=$\sqrt{2.5×1{0}^{-9}}$mol/L=5×10-5mol/L,二者混合后,钙离子浓度=2.5×10-5mol/L,草酸钾的浓度为4.0×10-4 mol/L,混合后c(Ca2+)•c (C2O42-)=2.5×10-5 ×4.0×10-4=1×10-8<Ksp(4.0×10-8),故无沉淀,故答案为:否.
点评 本题考查了盖斯定律、化学平衡的移动、化学平衡常数、电化学、难溶物的溶解平衡,明确溶度积常数的运用是解本题关键,难度中等.


 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:解答题
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2H4(g)+2H2O2(l)=N2(g)+4H2O(l)△H=+817.63 kJ•mol-1 | |
| B. | N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-641.63 kJ•mol-1 | |
| C. | N2H4(g)+2H2O2(l)=N2(g)+4H2O(l)△H=-641.63 kJ•mol-1 | |
| D. | N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-817.63 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过量CO2通入偏铝酸钠溶液中:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| B. | 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O═HClO+HSO${\;}_{3}^{-}$ | |
| C. | 酸性条件下双氧水和KI溶液反应:2I-+H2O2+2H+═I2+2H2O | |
| D. | 碳酸氢铵溶液与足量的KOH溶液混合后加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使酚酞变红色的溶液:Mg2+、K+、SO42-、NO3- | |
| B. | NaClO和NaCl混合溶液中:H+、NH4+、SO42-、Br- | |
| C. | 氯化亚铁溶液中:Na+、Ba2+、Br-、NO3- | |
| D. | 0.1 mol•L-1的NaAlO2 溶液:H+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若甲为AlCl3,则丁可能是NaOH | B. | 若甲为乙醇,则丙可能是乙酸 | ||
| C. | 若甲为Fe,则丁可能是稀硝酸 | D. | 若甲为NaOH 溶液,则丁可能是CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,CO2的结构式为O=C=O.
,CO2的结构式为O=C=O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgNO3溶液的浓度减小 | B. | 阳极上产生O2 | ||
| C. | 转移的电子数为0.02NA个 | D. | 阴极发生了氧化反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com