
����Ŀ���ⱻ��Ϊ������Ԫ�ء�����ѧ�����ز����ɷ��ε�ȱ������KI��KIO3���Ⱥ����ڼӵ����С�KI�������ڷ����Լ����й���ϡ���ҩ�ȣ����Ʊ�ԭ�����£�
��ӦI��3I2+ 6KOH== KIO3 +5KI+ 3H2O
��ӦII��3H2S+KIO3=3S��+KI+ 3H2O
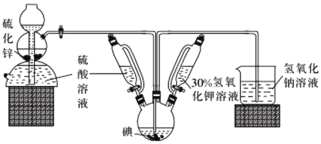
��ش��й����⡣
(1)���շ������з�����Ӧ�Ļ�ѧ����ʽΪ________��װ����ʢװ30%����������Һ������������__________��
(2)�ر����շ������������ȵ���30%��KOH��Һ.���۲쵽������ƿ����Һ��ɫ���ػ�ɫ��Ϊ______(������)��ֹͣ����KOH��Һ��Ȼ��________(�����)����������ƿ���ձ��в������ݵ����ʽӽ����ʱֹͣͨ����
(3)����������Һ������������ƿ�е���Һ����ˮԡ���ȣ���Ŀ����_______________��
(4)��������ƿ�е���Һ�����ձ��У�����̼�ᱵ���ڹ������й��ˣ����˵õ��ij����г����й���̼�ᱵ�⣬���������ᱵ��____(������)���ϲ���Һ��ϴ��Һ�������������ᾧ������ó�Ʒ��
(5)ʵ����ģ�ҵ�Ʊ�KIO3�������£�
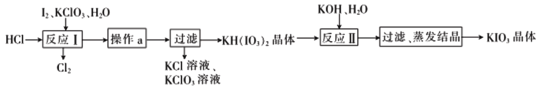
�������ʵ��ܽ�ȼ��±���
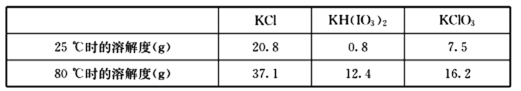
�ö��Ե缫���KI��ҺҲ���Ʊ�KIO3�����ⷨ��ȣ����������Ʊ�KIO3��ȱ����_________��
(6)ijͬѧ�ⶨ.��������������KIO3��Ʒ�Ĵ��ȡ�
ȡ1.00 g��Ʒ��������ˮ�в��������ữ���ټ��������KI�������ĵ�����Һ����εμ�2.0 mol��L-1 Na2S2O3��Һ��ǡ����ȫ��Ӧʱ������12. 60 mL Na2S2O3��Һ������Ʒ��KIO3����������Ϊ___________(��֪��Ӧ��I2+2Na2S2O3=2NaI+Na2S4O6)��
���𰸡�ZnS+H2SO4=H2S��+ZnSO4 ��ѹ��Һ©�� ��ɫ �����շ�����������ͨ������ ʹ��Һ�ữ�����ȣ���������Һ��ʣ��������ݳ����Ӷ���ȥ���� �� KClO3��I2��Ӧʱ������ж�����������Ⱦ���� 89.88%
��������
(1)���շ������з����ķ�Ӧ����п��ϡ���ᷴӦ�����������������п��
(2)������ƿ�����ȷ�����Ӧ3I2+ 6KOH= KIO3 +5KI+ 3H2O��Ȼ�������շ����������ɵ�H2S������Ӧ3H2S+KIO3=3S��+KI+ 3H2O���Ӷ��Ƶ�KI��
(1)���շ������з����ķ�Ӧ����п��ϡ���ᷴӦ�����������������п����Ӧ�Ļ�ѧ����ʽ�� ZnS+ H2SO4 =H2S��+ZnSO4������A������Ϊ��ѹ��Һ©�����ʴ�Ϊ�� ZnS+ H2SO4 =H2S��+ZnSO4����ѹ��Һ©����
(2)�ر����շ�������������Һ©���Ļ���������30%��KOH��Һ�����۲��ػ�ɫ��Һ��Ϊ��ɫ��ֹͣ����KOH��Һ��Ȼ������շ�����������ͨ�������KIO3���Һ��NaOH��Һ�������ʽӽ���ͬʱֹͣͨ�����ʴ�Ϊ����ɫ�������շ�����������ͨ�����壻
(3)����������Һ������KI���Һˮԡ���ȣ���Ŀ���ǣ�ʹ��Һ�ữ�����ȣ�������H2S������Ӷ���ȥH2S���ʴ�Ϊ��ʹ��Һ�ữ�����ȣ�������H2S������Ӷ���ȥH2S��
(4)ͨ�������KIO3���Һ��NaOH��Һ�������ʽӽ���ͬʱֹͣͨ�������з�����Ӧ3H2S+ KIO3 =3S��+KI+ 3H2O����KI���Һ�����ձ�������̼�ᱵ��ȥ���������ᣬ�ڹ������й��ˣ����˵õ��ij����г����й���̼�ᱵ�⣬�������ᱵ�͵����ʴ�Ϊ����
(5)�������̣��⡢����ء�ˮ�ữ��Ӧ�õ�KH(IO3)2��Cl2��KCl����ȥCl2���ᾧKH(IO3)2���ˣ�����KH(IO3)2��KCl����ˮ�ܽ�KH(IO3)2������KOH����pH��Ũ���ᾧ�õ�����أ���ⷨ��������Ϊ����أ���KClO3������������������Ⱦ�������ʴ�Ϊ��KClO3��I2��Ӧʱ������ж�����������Ⱦ������
(6)����Ʒ��KIO3����������Ϊx��
KIO3 + 5KI + 3H2SO4 = 3K2SO4 +3I2+3H2O�٣�I2+2S2O32-=2I- + S4O62-�ڣ�������ʽ�ڡ�3 +�ٵã�
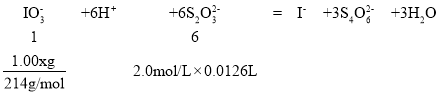
���Ե���ص���������x=![]() ���ʴ�Ϊ��89.88% ��
���ʴ�Ϊ��89.88% ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ʱ��
ʱ��![]() ��
��![]() ��
��![]() ����������10mL
����������10mL![]() ��Һ����μ���
��Һ����μ���![]() ��Һ����ͼ����Һ�к�̼Ԫ�������ʵ���������pH���Ͷ��仯��ͼ��
��Һ����ͼ����Һ�к�̼Ԫ�������ʵ���������pH���Ͷ��仯��ͼ��![]() �����ݳ�δ����
�����ݳ�δ����![]() ������˵���������
������˵���������
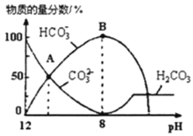
A.A����ʾ��Һ��![]()
B.B����ʾ��Һ��![]()
C.A��![]() �㷢����Ӧ�����ӷ���ʽΪ
�㷢����Ӧ�����ӷ���ʽΪ![]()
D.�ֲ������̪�ͼ��ȣ��õζ����ɲⶨ![]() ��
��![]() ���������
���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����ҺXֻ��������K+��NH4+��Cl-��Mg2+��Ba2+��CO32-��SO42-�е����������ӡ���ȡ����100mL����Һ��������ʵ�飺
��1�����һ����Һ�м���AgNO3��Һʱ�г���������
��2����ڶ�����Һ�м�������NaOH��Һ�����Ⱥ��ռ�������0.06mol��
��3�����������Һ�м�������BaCl2��Һ�����ó�����ϴ�ӡ��������Ϊ6.27g������������ϴ�ӡ������������Ϊ2.33g��
��������ʵ�飬�����Ʋ���ȷ����
A.K+һ������B.100mL��Һ�к�0.01mol CO32-
C.Cl���ܴ���D.Ba2+һ�������ڣ�Mg2+���ܴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ�����յ��о��Ŷ��Ƶ�һ������ˮϵп���,�ÿɳ������п����Һ��Ϊ���Һ,��ԭ����ͼ��ʾ������˵������ȷ����
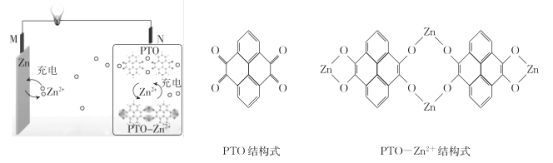
A.�ŵ�ʱ,N��������ԭ��Ӧ
B.���ʱ,Zn2+��M���ƶ�
C.�ŵ�ʱ,ÿ����1 mol PTO- Zn2+ ,M���ܽ�Zn������Ϊ260 g
D.���ʱ,N���ĵ缫��ӦʽΪ2PTO+8e- +4Zn2+=PTO- Zn2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵһ����֤��HNO2��������ʵ��ǣ� ��
�ٳ�����NaNO2��ҺpH����7
����HNO2��Һ������ʵ�飬���ݺܰ�
��HNO2��NaCl���ܷ�����Ӧ
��0.1![]() ��Һ��c(H+)Ϊ0.09
��Һ��c(H+)Ϊ0.09![]()
��NaNO2��![]() ��Ӧ������HNO2
��Ӧ������HNO2
A.�٢ڢ�B.�٢ڢ�
C.�٢ܢ�D.ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���������![]() ����
����![]()
ʯ��![]() �����Ʒ
�����Ʒ![]() ��ϩ
��ϩ![]() ��
��
A. ʯ����Ҫ��������ɵĻ����
B. ![]() ��Ҫ���������仯
��Ҫ���������仯
C. ![]() �����ѻ����ѽ�ȹ���
�����ѻ����ѽ�ȹ���
D. ![]() �Ǽӳɷ�Ӧ�����������Ƕ�������
�Ǽӳɷ�Ӧ�����������Ƕ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1 mol ����ϩ��![]() ���ڲ�ͬ��������H2�����ӳɷ�Ӧʱ��������ڲ��죺
���ڲ�ͬ��������H2�����ӳɷ�Ӧʱ��������ڲ��죺
���� | �������� | �ӳɲ��� | |
�� | ���¡���ѹ������ | 1 mol |
|
�� | ���¡���ѹ������ | 4 mol |
|
����˵����ȷ����
A.���������µļӳɲ��ﶼ���ڷ�����
B.���������µļӳɲ��ﶼ��ʹ���Ը��������Һ��ɫ
C.���������µļӳɲ��ﶼ���ڹ����������������ȡ��
D.������˵�������ϵ�̼̼˫���ȱ����ڵ�̼̼˫��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������״����������������������Ѿ���Ϊ��2020ÿ���˱ر�֮Ʒ�����粼���׳ƿ��ֵ������������ǿ����м�Ĺ��˲㣬�ܹ���ϸ������ֹ�������������粼��һ���Ը�����ָ���ľ۱�ϩ��PP��Ϊ���ϣ��������ݺύ������ά��������������ɵ�Ĥ�������йؾ۱�ϩ����ʶ��ȷ����
A.�ɱ�ϩͨ���Ӿ۷�Ӧ�ϳɾ۱�ϩ
B.�۱�ϩ�����ڣ���CH2��CH2��CH2��
C.�ϳɾ۱�ϩ�����ϩ�Ľṹ��ʽ��CH2CHCH3
D.�۱�ϩ��ʹ��ˮ�����ӳɷ�Ӧ����ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���������ڱ�������H2A��Ka1=1.1��10-3��Ka2=3.9��10-6����NaOH��Һ�ζ��ڱ���������أ�KHA����Һ�������Һ����Ե��������仯��ͼ��ʾ�����Ի��ʱ��Һ�¶ȵı仯��������N��Ϊ��Ӧ�յ㡣����˵����ȷ���ǣ� ��
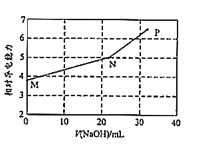
A.M������Ũ�ȣ�c��K+����c��HA-����c��H2A����c��A2-��
B.N����Һ�д��ڣ�c��Na+��+c��K+����2c��A2-��+2c��HA-��
C.P����Һ��һ�����ڣ�c��Na+����c��K+����c��OH-����c��A2-��
D.��M��P֮�����һ������ڣ�c��Na+��+c��K+��+c��H+��=c��A2-��+c��HA-��+c��OH-��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com